A | B | C | D | E | F | G | H | CH | I | J | K | L | M | N | O | P | Q | R | S | T | U | V | W | X | Y | Z | 0 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9

Keteny jsou organické sloučeniny se vzorcem R′R″C=C=O, kde R a R' jsou jednovazné funkční skupiny (nebo dvě oddělená substituční místa na stejné molekule).[1] Toto označení se také používá pro konkrétní sloučeninu ethenon H2C=C=O, který je nejjednodušším ketenem.[2][3]
Jedná se o velmi užitečnou skupinu sloučenin, přestože bývají nestálé. Při použití v chemických reakcích se obvykle připravují těsně před tím, než jsou potřeba.[1]
Historie
Keteny poprvé jako skupinu sloučenin zkoumal Hermann Staudinger roku 1905.[4] V tomto roce připravil difenylketen reakcí -chlordifenylacetylchloridu se zinkem. Staudinger toto provedl podle první přípravy organických meziproduktů, již provedl Moses Gomberg v roce 1900 (šlo o sloučeniny s trifenylmethylovými skupinami).[5]
Vlastnosti
Keteny jsou silně elektrofilní na uhlíkovém atomu sousedícím s heteroatomem, což je způsobeno sp hybridizací. Na sp uhlíky mohou být navázány atomy různých prvků, například kyslíku, síry nebo selenu, příslušné sloučeniny se nazývají keteny, thioketeny a selenoketeny.
Ethenon, nejjednodušší keten, má obě dvojné vazby různě dlouhé; délka vazby C=O činí 116,0 pm a u vazby C=C jde o 131,4 pm. Velikost úhlu mezi dvěma atomy uhlíku je 121,5°, podobná jako ideální úhel v molekule alkenu mezi sp2 uhlíkem a na něj navázanými vodíky.[6]
Keteny jsou nestabilní a nemohou být skladovány. Za nepřítomnosti nukleofilů, se kterými by mohl reagovat, tvoří ethenon dimer, kterým je β-lakton, tedy cyklický ester. U disubstituovaných ketenů jsou produkty dimerizace substiuované cyklobutadiony. Monosubstituované keteny mohou vytvořit estery nebo diketony.
Příprava
Ethenon lze připravit pyrolýzou acetonu:[7]
- CH3−CO−CH3 → CH2=C=O + CH4
Tato reakce se nazývá Schmidlinova syntéza ketenů.[8][9]
Ostatní keteny mohou být získány z acylchloridů eliminační reakcí, při níž se odštěpí chlorovodík (HCl):
Při této reakci zásada, například triethylamin, odštěpuje proton v poloze alfa vůči karbonylové skupině, čímž vyvolá vznik dvojné vazby mezi atomy uhlíku a odštěpení chloridového iontu:
Keteny lze připravit i Wolffovým přesmykem α-diazoketonů.
Další způsob přípravy představuje pyrolýza N-pyridylaminů. V roce 1997 byl vylepšen postup založený na pyrolýze vytvářející keteny za poměrně mírných podmínek (480 °C). N-pyridylaminy se získávají kondenzací R-malonátů s N-amino(pyrideny) v DCC.[10]
Keteny je také možné připravit karbonylací komplexů přechodných kovů s karbeny a přeměnou vzniklých vysoce reaktivních ketenů pomocí vhodných reaktantů, jako jsou iminy, aminy a alkoholy.[11] Jedná se o účinnou jednonádobovou karbonylaci řady α‐diazokarbonylových sloučenin a ketenů, které poté mohou reagovat s nukleofily a iminy za tvorby esterů, amidů a beta-laktamů. Lze při něm použít široké spektrum substrátů a různé kombinace karbenových prekurzorů, nukleofilů a iminů.[12]
Reakce a použití
Jelikož keteny obsahují kumulované dvojné vazby, tak jsou značně reaktivní.[13]
Vznik karboxylátových esterů
Reakcemi s alkoholy vznikají z ketenů estery karboxylových kyselin:
Vznik anhydridů karboxylových kyselin
S karboxylovými kyselinami keteny tvoří anhydridy karboxylových kyselin:
Vznik karboxamidů
Keteny reagují s amoniakem za vzniku primárních amidů:
Z primárních aminů obdobně vznikají sekundární amidy:
Reakce ketenů se sekundárními aminy vedou k tvorbě terciárních amidů:
Hydrolýza
Keteny lze hydrolyzovat na karboxylové kyseliny:
Vznik enolesterů
Enolestery se z ketenů dají získat reakcemi s enolizovatelnými karbonylovými sloučeninami. Na následujícím obrázku je uvedena reakce ethenonu s acetonem, jejímž produktem je propen-2-ylacetát:
Dimerizace
Za pokojové teploty se keteny rychle dimerizují na diketeny, ovšem zahřátím je lze získat zpět:
-cykloadice2+2-cykloadice" class="mw-editsection-visualeditor">editovat | editovat zdroj
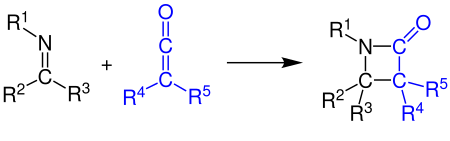
Keteny mohou reagovat s alkeny, karbonylovými sloučeninami, karbodiimidy a iminy 2+2 cykloadicích. Na následujícím obrázku je uvedena příprava β-laktamu reakcí ketenu s iminem (což je Staudingerova syntéza):[14][15]
Použitíeditovat | editovat zdroj
Keteny se vyznačují vysokou reaktivitou a jsou zapojeny do mnoha cykloadicí, jako je dimerizace na propiolaktony. Příkladem může být dimerizace ketenu kyseliny stearové za vzniku dimerních alkylketenů, které se používají v papírenském průmyslu.[1] Dimerní alkylketeny reagují s hydroxylovými skupinami celulózy a způsobují její esterifikaci.
Také vstupují do 2+2 cykloadicí s alkyny bohatými na elektrony za vzniku cyklobutenonů a s karbonylovými sloučeninami dávají beta-laktony. Reakcemi s iminy se tvoří beta-laktamy. Tato reakce, nazývaná Staudingerova syntéza, je průmyslově významnou reakcí.
S acetonem vzniká isopropenylacetát.[1]
Keteny mohou reagovat s hydroxylovými nukleofily za vzniku enolů nebo esterů, například reakcí ethenonu s vodou vzniká kyselina octová (přes ethen-1,1-diol) a s kyselinou octovou se vytváří acetanhydrid. Reakcemi diolů (HO−R−OH) a bisketenů (O=C=CH−R′−CH=C=O) vznikají polyestery typu (−O−R−O−CO−R′−CO)n.
Ethylacetacetát, významný výchozí materiál pro organické syntézy, může být získán reakcí diketenu a ethanolu. Vytváří se přímo ethylacetacetát s vysokou výtěžností; tento postup se používá i v průmyslu.
Odkazyeditovat | editovat zdroj
Související článkyeditovat | editovat zdroj
Externí odkazyeditovat | editovat zdroj
 Obrázky, zvuky či videa k tématu Keteny na Wikimedia Commons
Obrázky, zvuky či videa k tématu Keteny na Wikimedia Commons
Referenceeditovat | editovat zdroj
V tomto článku byl použit překlad textu z článku Ketene na anglické Wikipedii.
- ↑ a b c d Raimund Miller; Claudio Abaecherli; Adel Said; Barry Jackson. Ullmann's Encyclopedia of Industrial Chemistry. s.l.: s.n., 2001. ISBN 978-3527306732. DOI 10.1002/14356007.a15_063. Kapitola Ketenes.
- ↑ Saul Patai. Ketenes, Allenes and Related Compounds: Part 1, Volume 1. s.l.: John Wiley & Sons, 1980. ISBN 9780470771600. DOI 10.1002/9780470771600.
- ↑ Saul Patai. Ketenes, Allenes and Related Compounds: Part 2, Volume 2. s.l.: John Wiley & Sons, 1980. ISBN 9780471276708. DOI 10.1002/9780470771617.
- ↑ Hermann Staudinger. Ketene, eine neue Körperklasse. Berichte der Deutschen Chemischen Gesellschaft. 1905, s. 1735–1739. Dostupné online. DOI 10.1002/cber.19050380283.
- ↑ Thomas T. Tidwell, The first century of Ketenes (1905-2005): the birth of a family of reactive intermediates, Angewandte Chemie, Int. Edition, Band 44, 2005, S. 5778–5785
- ↑ Ngai Ling Ma; MingWah Wong. Theoretical Study of the Properties and Reactivities of Ketene, Thioketene, and Selenoketene. European Journal of Organic Chemistry. 2000, s. 1411–1421. Dostupné online. DOI 10.1002/(SICI)1099-0690(200004)2000:8<1411::AID-EJOC1411>3.0.CO;2-N. Archivováno 6. 11. 2021 na Wayback Machine.
- ↑ C. Weygand. Weygand/Hilgetag Preparative Organic Chemistry. Příprava vydání G. Hilgetag , A. Martini. New York: John Wiley & Sons, 1972. Dostupné online. ISBN 978-0471937494.
- ↑ C. D. Hurd; O. Kamm. Organic Syntheses. s.l.: s.n., 1941. Kapitola Ketene in Organic Syntheses.
- ↑ Julius Schmidlin; Maximilian Bergman. Darstellung des Ketens aus Aceton. Berichte der Deutschen Chemischen Gesellschaft. 1910, s. 2821–2823. Dostupné online. DOI 10.1002/cber.19100430340.
- ↑ Carsten Plüg; Hussein Kanaani; Curt Wentrup. Ketenes from N-(2-Pyridyl)amides. Australian Journal of Chemistry. 2015-02-12, s. 687. DOI 10.1071/CH14714.
- ↑ N. D. Paul; A. Chirila; H. Lu; X. P. Zhang; B. de Bruin. Carbene radicals in cobalt(II)-porphyrin-catalysed carbene carbonylation reactions; a catalytic approach to ketenes. Chemistry. 2013, s. 12953-12958. DOI 10.1002/chem.201301731. PMID 24038393.
- ↑ A. Chirila; K. M. van Vliet; N. D. Paul; B. de Bruin. Co(MeTAA) Metalloradical Catalytic Route to Ketenes via Carbonylation of Carbene Radicals. European Journal of Inorganic Chemistry. 2018, s. 2251–2258. Dostupné online. ISSN 1099-0682. DOI 10.1002/ejic.201800101.
- ↑ Siegfried Hauptmann. Organische Chemie: mit 65 Tabellen. s.l.: Deutscher Verlag für Grundstoffindustrie, 1985. ISBN 3871449024.
- ↑ Jie Jack Li. Name reactions. A collection of detailed reaction mechanisms. s.l.: Springer-Verlag, 2006. Dostupné online. ISBN 9783540300304. DOI 10.1007/3-540-30031-7. S. 561–562.
- ↑ Hermann Staudinger. Zur Kenntnis der Ketene. Diphenylketen. Justus Liebigs Annalen der Chemie. 1907, s. 51–123. Dostupné online. DOI 10.1002/jlac.19073560106.
Text je dostupný za podmienok Creative Commons Attribution/Share-Alike License 3.0 Unported; prípadne za ďalších podmienok. Podrobnejšie informácie nájdete na stránke Podmienky použitia.
Antény
Chemické zdroje elektriny
Chladenie v elektrotechnike
Elektrická sústava automobilu
Elektrická trakcia
Elektrické prístroje
Elektrické súčiastky
Elektrické spotrebiče
Elektrické stroje
Čítanie (elektrotechnika)
Činný výkon
Štatistická dynamika
Živý vodič
Admitancia
Antiparalelné zapojenie
Asynchrónny motor
Blúdivý prúd
Bočník (elektrotechnika)
Diak (polovodičový prvok)
Displej s kvapalnými kryštálmi
Elektrická inštalácia
Elektrická rezonancia
Elektrická sila
Elektrická vodivosť
Elektrické zariadenie
Elektrický obvod
Elektrický zvonec
Elektroenergetika
Elektromer
Elektrometer
Elektromobil
Elektromotor
Elektromotorické napätie
Elektrotechnický náučný slovník
Elektrotechnika
Elektrotechnológia
Fázor
Faradayova klietka
Frekvencia (fyzika)
Graetzov mostík
Impedancia
Indukčnosť
Induktancia
Istič
Izolácia (elektrotechnika)
Izolant
Jadro vodiča
Jednobran
Jednosmerný prúd
Joulovo teplo
Katóda
Koaxiálny kábel
Kompenzácia účinníka
Konduktometria
Konektor (elektrotechnika)
Korónový výboj
Lanko (elektrotechnika)
Leptanie
Logické hradlo
Magnetická susceptibilita
Magnetizácia (veličina)
Merný elektrický odpor
Mobilné zariadenie
Napájací zdroj
Napäťový chránič
Napäťový násobič
Nortonova veta
Odpínač
Odpojovač
OLED
Olovený akumulátor
Paralelné zapojenie
Peltierov článok
Plošná hustota elektrického prúdu
Poistka (elektrotechnika)
Posuvný prúd
Prúdový chránič
Prenosové médium
Prieletový klystrón
Primárny elektrochemický článok
Reaktancia
Rekuperácia (dopravný prostriedok)
Relé
Reproduktorová výhybka
Rezistancia
Rozhranie (interface)
Sériové zapojenie
Seebeckov jav
Sekundárny elektrochemický článok
Settopbox
Skrat
Sonar
Spínač
Spínaný zdroj
Straty v mikropásikových vedeniach
Striedavý prúd
Stupeň ochrany krytom
Svetelná výbojka
Symetrizačný člen
Technická normalizácia
Tepelné relé
Tepelne vodivostný detektor
Termočlánok
Théveninova veta
Transformátor
Transformátor s fázovou reguláciou
Trojfázová sústava
Tuhá fáza (elektronika)
Tyratrón
Usmerňovač (elektrotechnika)
Uzemnenie
Uzol (vodiče)
Vírivý prúd
Výbojka
Varistor
Ventilátor
Vodič (elektrotechnika)
Voltov stĺp
Vstavaný systém
Zásuvka (elektrotechnika)
Zdroj (elektrotechnika)
Zisk antény
Text je dostupný za podmienok Creative
Commons Attribution/Share-Alike License 3.0 Unported; prípadne za ďalších
podmienok.
Podrobnejšie informácie nájdete na stránke Podmienky
použitia.
www.astronomia.sk | www.biologia.sk | www.botanika.sk | www.dejiny.sk | www.economy.sk | www.elektrotechnika.sk | www.estetika.sk | www.farmakologia.sk | www.filozofia.sk | Fyzika | www.futurologia.sk | www.genetika.sk | www.chemia.sk | www.lingvistika.sk | www.politologia.sk | www.psychologia.sk | www.sexuologia.sk | www.sociologia.sk | www.veda.sk I www.zoologia.sk