A | B | C | D | E | F | G | H | CH | I | J | K | L | M | N | O | P | Q | R | S | T | U | V | W | X | Y | Z | 0 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9
Izomer je sloučenina téhož chemického složení (má stejný vzorec), ale rozdílné chemické struktury (má různou stereochemii).[1] Právě izomerie koordinačních sloučenin sehrála v jejich historii důležitou úlohu při objasňování jejich stereochemie. Přehled základních druhů izomerií je popsán níže.
Konformační izomerie
Konformační izomerie neboli polytopická izomerie přichází v úvahu pro každé koordinační číslo vyšší než tři a jakoukoliv jemu odpovídající geometrii. Izomery se navzájem liší pouze svou stereochemií. Např. existuje , který byl připraven jako zelený tetraedrický i jako žlutý čtvercový komplex. Konformační izomery musí mít srovnatelnou stabilitu, a aby je bylo možné od sebe oddělit, musí existovat dostatečně vysoká energetická bariéra pro jejich vzájemnou přeměnu. Tento druh izomerie nepatří mezi komplexy k úplně nejběžnějším, ale je možné se s ním v praxi setkat.
Konfrotační izomerie
Konfrotační izomerie vzniká při prohnutí chelátových kruhů jako například u ethan-1,2-diaminu. U pětičlenného kruhu vede tato izomerie ke dvěma enantiomerním uspořádáním. Tento druh izomerie je zvláštním druhem optické izomerie pro koordinační číslo 2 a nepatří k běžným druhům izomerie.
Geometrická izomerie
Geometrická izomerie vzniká u komplexů, jejichž koordinační číslo je větší než 3. S geometrickou izomerií se nejčastěji setkáváme u čtvercových komplexů typu a oktaedrických komplexů typu . V těch mohou ligandy (resp. jejich donorové atomy) obsadit sousední (cis neboli Z - z němčiny zusammen) nebo protilehlé vrcholy (trans neboli E - z němčiny entgegen). U oktaedrických komplexů typu mohou navíc existovat dvě geometrické formy lišící se polohou trojice donorových atomů. Ty mohou obsadit buď vrcholy jedné stěny oktaedru (fac - faciální uspořádání), nebo tři polohy na „obvodu“ oktaedru (mer - meridionální uspořádání). Čtvercové komplexy se čtyřmi různými ligandy pak mohou existovat ve třech geometricky izomerních formách, ale takové komplexy se s monodentátními ligandy velmi špatně připravují a jsou velmi vzácné. Geometrické izomery se liší v řadě fyzikálních vlastností, z nichž nejdůležitější pro diagnostické účely jsou dipólový moment a elektronová adsorpční spektra ve viditelné nebo ultrafialové oblasti.
Optická izomerieeditovat | editovat zdroj
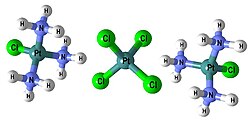
Optická izomerie vzniká u opticky aktivních látek. Optické izomery (enantiomery nebo antipody) lze očekávat u takových látek, v jejichž struktuře není žádný prvek symetrie kromě identity (nemají osu, rovinu ani střed symetrie). Takové látky, které se nazývají chirální (z řeckého chiros - ruka) nebo asymetrické, se mohou vyskytovat ve dvou formách, které se k sobě mají jako předmět a jeho obraz v zrcadle (nebo jako levá a pravá ruka). Takové dva izomery vypadají na první pohled zcela stejně, ovšem nelze je žádným otáčením a posunováním ztotožnit.
Významnou vlastností chirálních látek je jejich schopnost otáčet rovinu polarizovaného světla– jsou opticky aktivní. Enantiomery mají téměř všechny fyzikální a chemické vlastnosti stejné. Liší se pouze tím, že otáčejí rovinu polarizovaného světla (světlo, jehož vlny „kmitají“ jen v jednom směru) každý na jinou stranu. Podle toho se označují jako levotočivé (označované l nebo -) a pravotočivé (d nebo +) - dnes se již dřívější označování nesmí používat,[zdroj? jelikož otáčení roviny polarizovaného světla závisí na vlnové délce (Cottonově efektu). Dnes[kdy? se k označení chirality (absolutní konfigurace) používá Cahnova-Ingoldova-Prelogova symbolika R a S. Oba enantiomery se také mírně liší v indexu lomu a schopností absorbovat záření. Směs obou enantiomerů v molárním poměru 1 : 1 neotáčí rovinu polarizovaného světla a nazývá se racemická směs (racemát). Absolutní konfiguraci lze určit jedině kompletní rentgenostrukturní analýzou.
Optické izomery existují u čtvercových, tetraedrických a oktaedrických komplexů. U čtvercových komplexů je optická izomerie vzácná a může nastat pouze v případě vhodně nesymetrických ligandů. U tetraedrických komplexů by bylo možné očekávat větší rozšíření optické izomerie, protože každý tetraedrický komplex se čtyřmi různými ligandy musí být opticky aktivní. Takovéto komplexy je však obtížné připravit a tak i v tomto případě byly připraveny opticky aktivní látky pouze s vhodnými bidentátními ligandy. Nejčastěji se ovšem optická aktivita projevuje u oktaedrických komplexů s alespoň jedním chelátovým ligandem (například Cr(ox)32−, Co(edta)−, PtCl2(en)22+, Cr(NH3)2Cl2(en)). V podstatě každý oktaedrický komplex typu M(aa)3 nebo cis-M(aa)2L2 (kde aa je bidentátní ligand) může existovat ve dvou zrcadlově převrácených formách.
Pokud je ligand v takovém komplexu sám o sobě opticky aktivní (například 1,2-propandiamin), pak se počet možných optických izomerů zvyšuje. Izomerům se v takovém případě říká diastereoizomery. Ty už se mohou lišit i jinými vlastnostmi, jako jsou rozpustnost a stabilita.
-
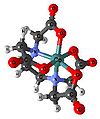
Cr(edta)−
-
Cr(edta)−
-
Cr(NH3)2Cl2(en)+
-
Cr(NH3)2Cl2(en)+
-
Cr(ox)32−
-
Cr(ox)32−
-
PtCl2(en)22+
-
PtCl2(en)22+
Ionizační izomerieeditovat | editovat zdroj
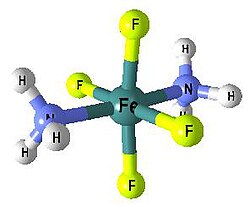
Ionizační izomerie vzniká, jestliže izomery poskytují v roztoku různé ionty. Jedná se o takové komplexní sloučeniny, které sestávají z komplexního kationtu a takového aniontu, který je sám o sobě potenciálním ligandem. Příkladem dvojice ionizačních izomerů jsou komplexy Pt(NH3)4Cl2Br2 a Pt(NH3)4Br2Cl2 nebo Co(NH3)5(SO4)Br a Co(NH3)5BrSO4.[2]
Hydrátová izomerieeditovat | editovat zdroj
Hydrátová izomerie je zvláštním případem ionizační izomerie a vzniká při rozdílné přítomnosti vody vázané uvnitř a mimo koordinační sféru. Typickým příkladem je hexahydrát chloridu chromitého CrCl3.6 H2O, který existuje ve třech izomerních formách: Cr(H2O)6Cl3 (fialový), Cr(H2O)5ClCl2.H2O (světle zelený) a Cr(H2O)4Cl2Cl.2 H2O (temně zelený). Izomery lze od sebe snadno odlišit srážecí reakcí s dusičnanem stříbrným AgNO3, který s jednotlivými izomery sráží 3, 2 nebo 1 iont Cl− jako chlorid stříbrný AgCl.
Vazebná izomerieeditovat | editovat zdroj
Vazebná izomerie vzniká, když se v komplexu váže ligand s větším počtem donorových atomů, které přitom nemůže použít současně (ambidentátní ligand). Při tom může teoreticky nastat situace, že se váže v jinak stejných sloučeninách jiným donorovým atomem. Situace, kdy se jeden ligand váže za různých okolností na centrální atom prostřednictvím rozdílných donorových atomů, ještě nemusí znamenat, že takové izomery jsou izolovatelné. Případy, kdy jsou takové izomery izolovatelné, jsou řídké a omezují se v podstatě na komplexy NO2− a SCN−. Příklady vazebných izomerů jsou dvojice Co(en)2(NO2)2+, Co(en)2(ONO)2+ a Pd(PPh3)2(NCS)2, Pd(PPh3)2(SCN)2. Abychom odlišili způsob vazby ligandů, uvádí se koordinovaný donorový atom ve vzorci jako první. Odlišují je též od sebe odlišným názvem nebo vyznačením donorového atomu. NO2− nazývá se nitro, ONO− nitrito, NCS− N-thiokyanato (izothiokyanato) a SCN− S-thiokyanato (thiokyanato).[3] Vazebné izomery se od sebe dají odlišit pomocí infračervené spektroskopie.[4]
Koordinační izomerieeditovat | editovat zdroj
Koordinační izomerie vzniká ve sloučeninách složených z komplexního kationtu i aniontu, který se může měnit rozdělením ligandů mezi oběma ionty. Počet takto vzniklých izomerů se dá ještě zvýšit dalšími kombinacemi ligandů, avšak takové složité koordinační izomery nejsou v uvedených případech známy. Ke koordinačním izomerů patří například Co(en)3Cr(CN)6 a Cr(en)3Co(CN)6 nebo PtII(NH3)4PtIVCl6 a PtIV(NH3)4Cl2PtIICl4. Izomery se v tomto případě liší fyzikálně-chemickými vlastnostmi.
Polohová izomerieeditovat | editovat zdroj
Polohová izomerie je zvláštním případem koordinační izomerie, která také vzniká kombinací ligandů, avšak tentokrát ve vícejaderných komplexech. Takovýto izomer je například (NH3)4Co(OH)2CO(NH3)2Cl22+ a (NH3)3ClCo(OH)2CO(NH3)3Cl2+.
Polymerační izomerieeditovat | editovat zdroj
Polymerační izomerie není izomerií v pravém slova smyslu. Některé komplexy existují ve formách jednoduchých (monomerních) a také jako dimery nebo trimery. Takové látky mají stejný sumární vzorec, ale liší se molekulovou hmotností. Např. látka sumárního vzorce Pt(NH3)2Cl2 existuje ve dvou monomerních formách (cis a trans), ale také jako dimer Pt(NH3)4PtCl4 a trimer Pt(NH3)3Cl2PtCl4. Komplexní částice Co(NH3)3(NO2)3 existuje v podobě sedmi sloučenin (kromě izomerů fac a mer). Polymerační izomery se liší chemickými a fyzikálními vlastnostmi.
Ligandová izomerieeditovat | editovat zdroj
Ligandová izomerie se vyskytuje u komplexů, jejichž izomery samy existují v izomerních podobách. Takovýto druh izomerie se vyskytuje například u komplexu Co(NH2C6H4Me)Cl(en)2Cl2, kde existují ortho- (o-), meta- (m-) a para- (p-) toluidin.
Odkazyeditovat | editovat zdroj
Referenceeditovat | editovat zdroj
- ↑ Chemické názvosloví anogranických sloučenin | PdF MU. is.muni.cz online. cit. 2022-06-13. Dostupné online.
- ↑ Structural Isomers - Ionization Isomerism in Transition Metal Complexes. Chemistry LibreTexts online. 2015-09-15 cit. 2022-06-13. Dostupné online. (anglicky)
- ↑ Rozlišení vazebných izomerů online. cit. 2022-06-13. Dostupné online.
- ↑ HEYNS, A.M.; DE WAAL, D. An infrared study of the nitro—nitrito linkage isomerization in solid nitro- and nitritopentamminecobalt(III) chloride. Spectrochimica Acta Part A: Molecular Spectroscopy. 1989-01, roč. 45, čís. 9, s. 905–909. Dostupné online cit. 2022-06-13. DOI 10.1016/0584-8539(89)80146-1. (anglicky)
Související článkyeditovat | editovat zdroj
- Koordinační chemie
- Ligand
- Centrální atom
- Koordinační vazba
- Komplexní sloučenina
- Koordinační číslo
- Barevnost komplexů
- Stabilita komplexních sloučenin
- Magnetické vlastnosti koordinačních sloučenin
Literaturaeditovat | editovat zdroj
- Dr. Heinrich Remy, Anorganická chemie 2. díl, 1. vydání 1961
- N. N. Greenwood - A. Earnshaw, Chemie prvků 2. díl, 1. vydání 1993 ISBN 80-85427-38-9
- Jursík F.: Anorganická chemie kovů. 1. vyd. 2002. ISBN 80-7080-504-8 (elektronická verze)
Text je dostupný za podmienok Creative Commons Attribution/Share-Alike License 3.0 Unported; prípadne za ďalších podmienok. Podrobnejšie informácie nájdete na stránke Podmienky použitia.
Antény
Chemické zdroje elektriny
Chladenie v elektrotechnike
Elektrická sústava automobilu
Elektrická trakcia
Elektrické prístroje
Elektrické súčiastky
Elektrické spotrebiče
Elektrické stroje
Čítanie (elektrotechnika)
Činný výkon
Štatistická dynamika
Živý vodič
Admitancia
Antiparalelné zapojenie
Asynchrónny motor
Blúdivý prúd
Bočník (elektrotechnika)
Diak (polovodičový prvok)
Displej s kvapalnými kryštálmi
Elektrická inštalácia
Elektrická rezonancia
Elektrická sila
Elektrická vodivosť
Elektrické zariadenie
Elektrický obvod
Elektrický zvonec
Elektroenergetika
Elektromer
Elektrometer
Elektromobil
Elektromotor
Elektromotorické napätie
Elektrotechnický náučný slovník
Elektrotechnika
Elektrotechnológia
Fázor
Faradayova klietka
Frekvencia (fyzika)
Graetzov mostík
Impedancia
Indukčnosť
Induktancia
Istič
Izolácia (elektrotechnika)
Izolant
Jadro vodiča
Jednobran
Jednosmerný prúd
Joulovo teplo
Katóda
Koaxiálny kábel
Kompenzácia účinníka
Konduktometria
Konektor (elektrotechnika)
Korónový výboj
Lanko (elektrotechnika)
Leptanie
Logické hradlo
Magnetická susceptibilita
Magnetizácia (veličina)
Merný elektrický odpor
Mobilné zariadenie
Napájací zdroj
Napäťový chránič
Napäťový násobič
Nortonova veta
Odpínač
Odpojovač
OLED
Olovený akumulátor
Paralelné zapojenie
Peltierov článok
Plošná hustota elektrického prúdu
Poistka (elektrotechnika)
Posuvný prúd
Prúdový chránič
Prenosové médium
Prieletový klystrón
Primárny elektrochemický článok
Reaktancia
Rekuperácia (dopravný prostriedok)
Relé
Reproduktorová výhybka
Rezistancia
Rozhranie (interface)
Sériové zapojenie
Seebeckov jav
Sekundárny elektrochemický článok
Settopbox
Skrat
Sonar
Spínač
Spínaný zdroj
Straty v mikropásikových vedeniach
Striedavý prúd
Stupeň ochrany krytom
Svetelná výbojka
Symetrizačný člen
Technická normalizácia
Tepelné relé
Tepelne vodivostný detektor
Termočlánok
Théveninova veta
Transformátor
Transformátor s fázovou reguláciou
Trojfázová sústava
Tuhá fáza (elektronika)
Tyratrón
Usmerňovač (elektrotechnika)
Uzemnenie
Uzol (vodiče)
Vírivý prúd
Výbojka
Varistor
Ventilátor
Vodič (elektrotechnika)
Voltov stĺp
Vstavaný systém
Zásuvka (elektrotechnika)
Zdroj (elektrotechnika)
Zisk antény
Text je dostupný za podmienok Creative
Commons Attribution/Share-Alike License 3.0 Unported; prípadne za ďalších
podmienok.
Podrobnejšie informácie nájdete na stránke Podmienky
použitia.
www.astronomia.sk | www.biologia.sk | www.botanika.sk | www.dejiny.sk | www.economy.sk | www.elektrotechnika.sk | www.estetika.sk | www.farmakologia.sk | www.filozofia.sk | Fyzika | www.futurologia.sk | www.genetika.sk | www.chemia.sk | www.lingvistika.sk | www.politologia.sk | www.psychologia.sk | www.sexuologia.sk | www.sociologia.sk | www.veda.sk I www.zoologia.sk