A | B | C | D | E | F | G | H | CH | I | J | K | L | M | N | O | P | Q | R | S | T | U | V | W | X | Y | Z | 0 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9
| Chlorid chromitý | |||||||||||||||||||||||||||||||||
 | |||||||||||||||||||||||||||||||||
 | |||||||||||||||||||||||||||||||||
| Všeobecné vlastnosti | |||||||||||||||||||||||||||||||||
| Sumárny vzorec | CrCl3 | ||||||||||||||||||||||||||||||||
| Vzhľad | fialový prášok (bezvodný) tmavozelené, zelené alebo fialové kryštály (hexahydrát) | ||||||||||||||||||||||||||||||||
| Fyzikálne vlastnosti | |||||||||||||||||||||||||||||||||
| Molekulová hmotnosť | 158,4 u (bezvodný) 266,5 u (hexahydrát) | ||||||||||||||||||||||||||||||||
| Molárna hmotnosť | 158,355 g/mol (bezvodný) 266,48 g/mol (hexahydrát) | ||||||||||||||||||||||||||||||||
| Teplota topenia | 1 150 °C (pri zvýšenom tlaku) 83 °C (hexahydrát) | ||||||||||||||||||||||||||||||||
| Teplota rozkladu | 1 300 °C | ||||||||||||||||||||||||||||||||
| Hustota | 2,915 6 g/cm³ (bezvodný) 1,760 g/cm³ (hexahydrát) | ||||||||||||||||||||||||||||||||
| Rozpustnosť | vo vode: takmer nerozpustný v polárnych rozpúšťadlách: Metanol Dietyléter Acetón | ||||||||||||||||||||||||||||||||
| Termochemické vlastnosti | |||||||||||||||||||||||||||||||||
| Štandardná zlučovacia entalpia | -563,3 kJ/mol | ||||||||||||||||||||||||||||||||
| Štandardná entropia | 125,6 J K-1 mol-1 | ||||||||||||||||||||||||||||||||
| Štandardná Gibbsová energia | -493,8 kJ/mol | ||||||||||||||||||||||||||||||||
| Merná tepelná kapacita | 0,580 J K-1 g-1 | ||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||
| Ďalšie informácie | |||||||||||||||||||||||||||||||||
| Číslo CAS | 10025-73-7 10060-12-5 (hexahydrát) | ||||||||||||||||||||||||||||||||
| EINECS číslo | 233-038-3 | ||||||||||||||||||||||||||||||||
| Číslo RTECS | GB5425000 | ||||||||||||||||||||||||||||||||
| Pokiaľ je to možné a bežné, používame jednotky sústavy SI. Ak nie je hore uvedené inak, údaje sú za normálnych podmienok. | |||||||||||||||||||||||||||||||||
Chlorid chromitý (CrCl3) tvorí v bezvodom stave červenofialové (broskyňovo) lesklé lístočky, ktoré možno pri červenom svetle v prúde chlóru prečisťovať sublimáciou. Bez prítomnosti chlóru dochádza k čiastočnému rozkladu na chlorid chromnatý a chlór. Vo vode a etanole sa rozpúšťa veľmi obmedzene a to aj za varu. Rozpúšťa sa však, ak je v kvapaline prítomné aspoň malé množstvo chloridu chromnatého a to dokonca za uvoľňovania tepla (vzniká tmavozelený roztok hexahydrátu). Rozpustnejší je ďalej aj bez pridania chloridu chromnatého v metanole, dietyléteri a acetóne. Má sladkastú chuť. Hydráty majú zložitejšiu komplexnú povahu a ich štruktúra je podrobnejšie popísaná nižšie.
Hydráty chloridu chromitého

Z vodného roztoku kryštalizuje tmavozelený hexahydrát chloridu chromitého CrCl3 • 6 H2O, ktorý má oktaedrické ligandové pole okolo centrálneho atómu Cr3+. Zráža sa reakciou s dusičnanom strieborným podľa stechiometrickej reakcie zrazí len jeden z prítomných chloridových aniónov, čo znamená, že zvyšné 2 musia byť vo zlúčenine viazané komplexne. Štruktúrne správny zápis vzorca vystihuje preto tvar Cl • 2 H2O, systematicky sa táto zlúčenina potom nazýva dihydrát chloridu tetraaqua-dichloridochromitého. Okrem tejto zlúčeniny, ktorú možno považovať za hexahydrát chloridu chromitého, existujú však aj jej ďalšie 2 hydrátové izoméry.
Existuje ďalej zelená zlúčenina so vzorcom Cl2 • H2O (hydrát dichloridu pentaaqua-chloridochromitého) a sivomodrý Cl3 (trichlorid hexaaquachromitý). Rozlíšenie týchto zlúčenín od seba sa vykonáva už vyššie spomenutým zrážaním s dusičnanom strieborným a podľa množstva zrazeného chloridu strieborného je možné zo stechiometrickej rovnice jednoducho vypočítať, o ktorý z týchto hydrátov ide:
- Cl + 3 AgNO3 → NO3 + 2 AgNO3 + AgCl↓
- Cl2 + 3 AgNO3 → (NO3)2 + AgNO3 + 2 AgCl↓
- Cl3 + 3 AgNO3 → (NO3)3 + 3 AgCl↓
Ak sa nechá chlorid chromitý kryštalizovať z roztokov ochladzovaných pod 6 °C, tak z nich kryštalizuje v podobe dekahydrátu chloridu chromitého CrCl3 • 10 H2O.
Príprava
V bezvodom stave je možné chlorid chromitý pripraviť vedením suchého chlóru cez kovový chróm zahriaty do červeného žiaru. Jedná sa síce o exotermickú reakciu, tá však neprodukuje toľko tepla, aby sa následne sama udržala v chode:
- 2 Cr + 3 Cl2 → 2 CrCl3
Ďalším spôsobom prípravy je vedenie suchého chlóru cez zmes oxidu chromitého Cr2O3 a uhlie zahriatych k žiaru:
- Cr2O3 + 3 C + 3 Cl2 → 2 CrCl3 + 3 CO
Ďalšou možnosťou je zahrievanie oxidu chromitého s chloridom uhličitým CCl4 alebo dichloridom disírnatým S2Cl2:
- Cr2O3 + 3 CCl4 → 2 CrCl3 + COCl2
- 2 Cr2O3 + 6 S2Cl2 + 9 O2 → 4 CrCl3 + 12 SO2
Reakcia a použitie
Bezvodý chlorid chromitý reaguje s inými zlúčeninami za vzniku ďalších chromitých zlúčenín. Žíhaním na vzduchu prechádza do zeleného oxidu chromitého. Pôsobením sírovodíka H2S, amoniaku NH3 alebo fosfánu PH3 za žiaru ho možno previesť na zlúčeniny s príslušným aniónom.
- 4 CrCl3 + 3 O2 → 2 Cr2O3 + 6 Cl2
- 2 CrCl3 + 3 H2S → Cr2S3 + 6 HCl
- CrCl3 + NH3 → CrN + 3 HCl
- CrCl3 + PH3 → CrP + 3 HCl
Chlorid chromitý je Lewisovou kyselinou, ktorá patrí tzv. tvrdé kyseliny a tvorí veľmi často zlúčeniny typu , kde L je Lewisova báza. Napríklad reakciou s pyridínom vzniká adukt:
- CrCl3 + 3 C5H5N →
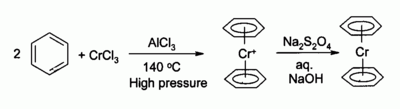
S roztavenými chloridmi alkalických kovov, ako napríklad chloridom draselným, dáva chlorid chromitý oktaedrické komplexy typu hexachloridochromitanu draselného K3 alebo pri väčšom množstve chloridu chromitého dáva nonachloridochromitan draselný CrCl3K3, ktorý je tiež oktaedrický, ale v ktorom sú 2 atómy chrómu spojené cez 3 atómy chlóru mostíkovou väzbou. Chlorid chromitý sa používa ako prekurzor pre veľké množstvo zlúčenín, napríklad bis(benzén)chrómu, analóg ferocénu:
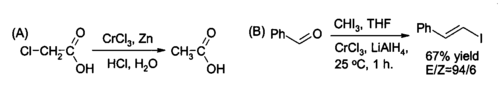
Jedno z použití chloridu chromitého v organickej syntéze je jeho redukcia na chlorid chromnatý CrCl2 priamo v reakčnej zmesi a používa sa ako činidlo na (A) redukciu alkyl halogenidov a (B) syntézu (trans)-alkenyl halogenidov. Reakcia sa zvyčajne vykonáva pomocou dvoch molov chloridu chromitého na mol tetrahydridohlinitanu lítneho Li, aj keď v prípade vodného roztoku stačí zinok a kyselina chlorovodíková.
Chlorid chromitý sa ako Lewisova kyselina takisto využíva na katalýzu nitrózo Diels-Alderových reakcií.
Podobné látky
- Bromid chromitý
- Fluorid chromitý
- Jodid chromitý
- Chlorid chromičitý
- Chlorid chrómnatý
- Chlorid molybdénitý
- Chlorid volfrámitý
Zdrojupraviť | upraviť zdroj
Tento článok je čiastočný alebo úplný preklad článku Chlorid chromitý na českej Wikipédii.
Literatúraupraviť | upraviť zdroj
- VOHLÍDAL, Jiří; ŠTULÍK, Karel; JULÁK, Alois. Chemické a analytické tabuľky. 1. vyd. Praha : Grada Publishing, 1999. ISBN 80-7169-855-5.
- Dr. Heinrich Remy, Anorganická chémia, 2. diel. Preklad Milan Drátovský, Zdeněk Hauptman, Jiří Hejduk, Vladimír Machálek, Lieselotta Pačesová. 1. vyd. Praha : SNTL, 1961. (český)
Text je dostupný za podmienok Creative Commons Attribution/Share-Alike License 3.0 Unported; prípadne za ďalších podmienok. Podrobnejšie informácie nájdete na stránke Podmienky použitia.
Antény
Chemické zdroje elektriny
Chladenie v elektrotechnike
Elektrická sústava automobilu
Elektrická trakcia
Elektrické prístroje
Elektrické súčiastky
Elektrické spotrebiče
Elektrické stroje
Čítanie (elektrotechnika)
Činný výkon
Štatistická dynamika
Živý vodič
Admitancia
Antiparalelné zapojenie
Asynchrónny motor
Blúdivý prúd
Bočník (elektrotechnika)
Diak (polovodičový prvok)
Displej s kvapalnými kryštálmi
Elektrická inštalácia
Elektrická rezonancia
Elektrická sila
Elektrická vodivosť
Elektrické zariadenie
Elektrický obvod
Elektrický zvonec
Elektroenergetika
Elektromer
Elektrometer
Elektromobil
Elektromotor
Elektromotorické napätie
Elektrotechnický náučný slovník
Elektrotechnika
Elektrotechnológia
Fázor
Faradayova klietka
Frekvencia (fyzika)
Graetzov mostík
Impedancia
Indukčnosť
Induktancia
Istič
Izolácia (elektrotechnika)
Izolant
Jadro vodiča
Jednobran
Jednosmerný prúd
Joulovo teplo
Katóda
Koaxiálny kábel
Kompenzácia účinníka
Konduktometria
Konektor (elektrotechnika)
Korónový výboj
Lanko (elektrotechnika)
Leptanie
Logické hradlo
Magnetická susceptibilita
Magnetizácia (veličina)
Merný elektrický odpor
Mobilné zariadenie
Napájací zdroj
Napäťový chránič
Napäťový násobič
Nortonova veta
Odpínač
Odpojovač
OLED
Olovený akumulátor
Paralelné zapojenie
Peltierov článok
Plošná hustota elektrického prúdu
Poistka (elektrotechnika)
Posuvný prúd
Prúdový chránič
Prenosové médium
Prieletový klystrón
Primárny elektrochemický článok
Reaktancia
Rekuperácia (dopravný prostriedok)
Relé
Reproduktorová výhybka
Rezistancia
Rozhranie (interface)
Sériové zapojenie
Seebeckov jav
Sekundárny elektrochemický článok
Settopbox
Skrat
Sonar
Spínač
Spínaný zdroj
Straty v mikropásikových vedeniach
Striedavý prúd
Stupeň ochrany krytom
Svetelná výbojka
Symetrizačný člen
Technická normalizácia
Tepelné relé
Tepelne vodivostný detektor
Termočlánok
Théveninova veta
Transformátor
Transformátor s fázovou reguláciou
Trojfázová sústava
Tuhá fáza (elektronika)
Tyratrón
Usmerňovač (elektrotechnika)
Uzemnenie
Uzol (vodiče)
Vírivý prúd
Výbojka
Varistor
Ventilátor
Vodič (elektrotechnika)
Voltov stĺp
Vstavaný systém
Zásuvka (elektrotechnika)
Zdroj (elektrotechnika)
Zisk antény
Text je dostupný za podmienok Creative
Commons Attribution/Share-Alike License 3.0 Unported; prípadne za ďalších
podmienok.
Podrobnejšie informácie nájdete na stránke Podmienky
použitia.
www.astronomia.sk | www.biologia.sk | www.botanika.sk | www.dejiny.sk | www.economy.sk | www.elektrotechnika.sk | www.estetika.sk | www.farmakologia.sk | www.filozofia.sk | Fyzika | www.futurologia.sk | www.genetika.sk | www.chemia.sk | www.lingvistika.sk | www.politologia.sk | www.psychologia.sk | www.sexuologia.sk | www.sociologia.sk | www.veda.sk I www.zoologia.sk