A | B | C | D | E | F | G | H | CH | I | J | K | L | M | N | O | P | Q | R | S | T | U | V | W | X | Y | Z | 0 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9
Acylchloridy jsou organické sloučeniny s molekulami obsahujícími skupinu -COCl; jedná se o reaktivní funkční deriváty karboxylových kyselin. Acylchloridy patří mezi acylhalogenidy.
Názvosloví
Pokud je acyl hlavní skupinou, tak se acylchloridy pojmenovávají podle názvu tohoto acylu, ke kterému se přidá označení -chlorid, například:
Pokud acyl není hlavní skupinou, tak se používá předpona -chlorkarbonyl, například:
- kyselina (chlorkarbonyl)octová ClOCCH2COOH
Vlastnosti
Jelikož u acylchloridů nedochází k tvorbě vodíkových vazeb, tak mají tyto látky nižší teploty varu a tání než odpovídající karboxylové kyseliny; teplota varu kyseliny octové je 118 °C, zatímco acetylchlorid vře již při 51 °C.
Podobně jako většina karbonylových sloučenin mají acylchloridy v infračervených spektrech výrazný absorpční pás kolem hodnoty vlnočtu 1750 cm−1.
Nejjednodušším stabilním acylchloridem je acetylchlorid (systematickým názvem ethanoylchlorid); formylchlorid (methanoylchlorid) je za běžných podmínek nestabilní, lze jej však připravit za teplot pod -60 °C.[1][2]
Výroba a příprava
V průmyslu
Průmyslově se acylchloridy vyrábějí reakcí acetanhydridu s chlorovodíkem. U benzoylchloridu se používá částečná hydrolýza benzotrichloridu:[3]
- C6H5CCl3 + H2O → C6H5C(O)Cl + 2 HCl
V laboratořích
Laboratorně se acylchloridy, podobně jako chlorované uhlovodíky, získávají nahrazením hydroxylových skupin atomy chloru: karboxylová kyselina reaguje s chloridem thionylu (SOCl2),[4] chloridem fosforitým (PCl3)[5] nebo chloridem fosforečným (PCl5):[6][7]
- RCOOH + SOCl2 → RCOCl + SO2 + HCl
- 3 RCOOH + PCl3 → 3 RCOCl + H3PO3
- RCOOH + PCl5 → RCOCl + POCl3 + HCl
Reakci s chloridem thionylu je možné katalyzovat dimethylformamidem.[8] Při tomto postupu vznikají oxid siřičitý a chlorovodík, což jsou plyny, které se z reakční směsi odstraňují a tím dochází k posunu reakční rovnováhy ve prospěch produktů. Přebytek thionylchloridu, jehož teplota varu činí 74,6 °C, lze taktéž snadno odstranit.[7] Mechanismy reakcí s thionylchloridem a chloridem fosforečným jsou podobné; níže je zobrazen mechanismus při použití thionylchloridu:[8]
Při jiné metodě se používá oxalylchlorid:
- RCOOH + ClCOCOCl → RCOCl + CO + CO2 + HCl
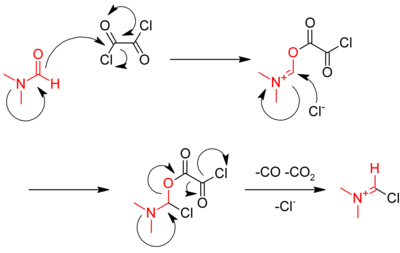
Katalyzátorem je zde dimethylformamid, který na začátku reaguje s oxalylchloridem za vzniku iminiového meziproduktu,
který poté reaguje s karboxylovou kyselinou, přičemž dochází k odštěpení oxidu a obnovení katalyzátoru.
Jsou známy i takové postupy přípravy acylchloridů, při kterých nevzniká HCl, jako jsou například Appelova reakce[9]
- RCOOH + Ph3P + CCl4 → RCOCl + Ph3PO + HCCl3
a příprava za použití trichlortriazinu:[10]
Reakce
Nukleofilní reakce
Acylchloridy jsou mnohem reaktivnější než karboxylové kyseliny; chloridový aniont je velmi dobrou odcházející skupinou, zatímco hydroxid tuto vlastnost za obvyklých podmínek nemá, a tak mohou s karbonylovou skupinou reagovat i slabé nukleofily; příkladem může být reakce s vodou za vzniku příslušné karboxylové kyseliny:
- RCOCl + H2O → RCO2H + HCl
Acylchloridy lze použít na přípravu derivátů karboxylových kyselin jako jsou anhydridy, estery a amidy, reakcemi se solemi příslušných kyselin, alkoholy či aminy. Za přítomnosti zásady, například vodného roztoku hydroxidu sodného nebo pyridinu,[7] případně přebytku aminu (při přípravě amidů),[8] je potřeba odstraňovat vznikající chlorovodík a reakce musí být katalyzována. I když lze estery či amidy často získat reakcí karboxylové kyseliny s alkoholem nebo aminem, tak jsou tyto reakce vratné, což vede k nízké výtěžnosti; příprava těchto látek z acylchloridů je rychlá a nevratná a tak se často upřednostňuje před přímou reakcí s karboxylovou kyselinou.[7]
Při reakcích acylchloridů s Grignardovými činidly se obvykle nejprve tvoří ketony a následně terciární alkoholy; výjimku představují reakce s některými organickými sloučeninami kadmia, při nichž se proces zastaví u ketonu. Nukleofilní reakce s Gilmanovými činidly (organickými sloučeninami obsahujícími lithium a měď) také, díky nižší reaktivitě těchto látek, poskytují ketony.[7] Chloridy aromatických kyselin jsou obecně méně reaktivní než chloridy alkylových kyselin a často jsou tak potřeba tvrdší podmínky.
Acylchloridy je možné zredukovat silnými donory hydridů, jako je hydrid lithno-hlinitý, za tvorby primárních alkoholů. Tri-terc-butoxyhydrid lithnohlinitý přeměňuje acylchloridy na aldehydy.[11]
Elektrofilní reakce
Acylchloridy se, společně s Lewisovými kyselinami, jako například chloridem železitým a chloridem hlinitým, účastní Friedelových–Craftsových acylací, při nichž vznikají arylketony.[5][7]
V prvním kroku proběhne disociace chloridu, kterou vyvolá Lewisova kyselina:
Poté následuje nukleofilní atak arenu na acylovou skupinu:
Nakonec nastane spojení chloridového aniontu s uvolněným protonem za vzniku HCl a regenerace katalyzátoru (zde AlCl3):
Bezpečnost
Vzhledem ke značné reaktivitě těchto látek je při skladování acylchloridů nutné opatrné zacházení. Mají dráždivé účinky na oči, jelikož reagují s vodou za vzniku chlorovodíku a organických kyselin.
Reference
V tomto článku byl použit překlad textu z článku Acyl chloride na anglické Wikipedii.
- ↑ John C. Sih. Encyclopedia of Reagents for Organic Synthesis. New York: John Wiley & Sons, 15. 4. 2001. Dostupné online. ISBN 9780471936237. Kapitola Formyl Chloride. (anglicky)
- ↑ Richard O.C. Norman; James M. Coxon. Principles of Organic Synthesis. : CRC Press, 16. 9. 1993. (3). ISBN 978-0-7487-6162-3. S. 371. (anglicky)
- ↑ Takao Maki, Kazuo Takeda “Benzoic Acid and Derivatives” Ullmann's Encyclopedia of Industrial Chemistry 2002, Wiley-VCH, Weinheim. DOI: 10.1002/14356007.a03_555
- ↑ B. Helferich; W. Schaefer. n-Butyrl chloride. Organic Syntheses. 1929, s. 32. (anglicky)
- ↑ a b C. F. H. Allen; W.E. Barker. Desoxybenzoin. Organic Syntheses. 1932, s. 16.
- ↑ Roger Adams. p-Nitrobenzoyl chloride. Organic Syntheses. 1923, s. 75. (anglicky)
- ↑ a b c d e f Robert W. Boyd; Robert Morrison. Organic chemistry. : Prentice Hall, 1992. Dostupné online. ISBN 0-13-643669-2. S. 666–762. (anglicky)
- ↑ a b c Jonathan Clayden. Organic chemistry. : Oxford University Press, 2001. Dostupné online. ISBN 0-19-850346-6. S. 276–296. (anglicky)
- ↑ "Triphenylphosphine-carbon tetrachloride Archivováno 23. 3. 2010 na Wayback Machine. Taschner, Michael J. e-EROS: Encyclopedia of Reagents for Organic Synthesis, 2001
- ↑ K. Venkataraman; D. R. Wagle. Cyanuric chloride : a useful reagent for converting carboxylic acids into chlorides, esters, amides and peptides. Tetrahedron Letters. 1979, s. 3037–3040. (anglicky)
- ↑ William Reusch. Carboxylic Acid Derivatives . Michiganská státní univerzita . Dostupné v archivu pořízeném dne 2016-05-16.
Externí odkazy
 Obrázky, zvuky či videa k tématu Acylchloridy na Wikimedia Commons
Obrázky, zvuky či videa k tématu Acylchloridy na Wikimedia Commons
Text je dostupný za podmienok Creative Commons Attribution/Share-Alike License 3.0 Unported; prípadne za ďalších podmienok. Podrobnejšie informácie nájdete na stránke Podmienky použitia.
Antény
Chemické zdroje elektriny
Chladenie v elektrotechnike
Elektrická sústava automobilu
Elektrická trakcia
Elektrické prístroje
Elektrické súčiastky
Elektrické spotrebiče
Elektrické stroje
Čítanie (elektrotechnika)
Činný výkon
Štatistická dynamika
Živý vodič
Admitancia
Antiparalelné zapojenie
Asynchrónny motor
Blúdivý prúd
Bočník (elektrotechnika)
Diak (polovodičový prvok)
Displej s kvapalnými kryštálmi
Elektrická inštalácia
Elektrická rezonancia
Elektrická sila
Elektrická vodivosť
Elektrické zariadenie
Elektrický obvod
Elektrický zvonec
Elektroenergetika
Elektromer
Elektrometer
Elektromobil
Elektromotor
Elektromotorické napätie
Elektrotechnický náučný slovník
Elektrotechnika
Elektrotechnológia
Fázor
Faradayova klietka
Frekvencia (fyzika)
Graetzov mostík
Impedancia
Indukčnosť
Induktancia
Istič
Izolácia (elektrotechnika)
Izolant
Jadro vodiča
Jednobran
Jednosmerný prúd
Joulovo teplo
Katóda
Koaxiálny kábel
Kompenzácia účinníka
Konduktometria
Konektor (elektrotechnika)
Korónový výboj
Lanko (elektrotechnika)
Leptanie
Logické hradlo
Magnetická susceptibilita
Magnetizácia (veličina)
Merný elektrický odpor
Mobilné zariadenie
Napájací zdroj
Napäťový chránič
Napäťový násobič
Nortonova veta
Odpínač
Odpojovač
OLED
Olovený akumulátor
Paralelné zapojenie
Peltierov článok
Plošná hustota elektrického prúdu
Poistka (elektrotechnika)
Posuvný prúd
Prúdový chránič
Prenosové médium
Prieletový klystrón
Primárny elektrochemický článok
Reaktancia
Rekuperácia (dopravný prostriedok)
Relé
Reproduktorová výhybka
Rezistancia
Rozhranie (interface)
Sériové zapojenie
Seebeckov jav
Sekundárny elektrochemický článok
Settopbox
Skrat
Sonar
Spínač
Spínaný zdroj
Straty v mikropásikových vedeniach
Striedavý prúd
Stupeň ochrany krytom
Svetelná výbojka
Symetrizačný člen
Technická normalizácia
Tepelné relé
Tepelne vodivostný detektor
Termočlánok
Théveninova veta
Transformátor
Transformátor s fázovou reguláciou
Trojfázová sústava
Tuhá fáza (elektronika)
Tyratrón
Usmerňovač (elektrotechnika)
Uzemnenie
Uzol (vodiče)
Vírivý prúd
Výbojka
Varistor
Ventilátor
Vodič (elektrotechnika)
Voltov stĺp
Vstavaný systém
Zásuvka (elektrotechnika)
Zdroj (elektrotechnika)
Zisk antény
Text je dostupný za podmienok Creative
Commons Attribution/Share-Alike License 3.0 Unported; prípadne za ďalších
podmienok.
Podrobnejšie informácie nájdete na stránke Podmienky
použitia.
www.astronomia.sk | www.biologia.sk | www.botanika.sk | www.dejiny.sk | www.economy.sk | www.elektrotechnika.sk | www.estetika.sk | www.farmakologia.sk | www.filozofia.sk | Fyzika | www.futurologia.sk | www.genetika.sk | www.chemia.sk | www.lingvistika.sk | www.politologia.sk | www.psychologia.sk | www.sexuologia.sk | www.sociologia.sk | www.veda.sk I www.zoologia.sk