A | B | C | D | E | F | G | H | CH | I | J | K | L | M | N | O | P | Q | R | S | T | U | V | W | X | Y | Z | 0 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9
| Hexakarbonyl vanadu | |
|---|---|
 Strukturní vzorec | |
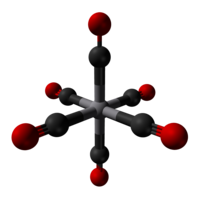 Krystalová struktura | |
| Obecné | |
| Systematický název | Hexakarbonyl vanadu |
| Anglický název | Vanadium hexacarbonyl |
| Německý název | Vanadiumhexacarbonyl |
| Sumární vzorec | V(CO)6 |
| Vzhled | modrozelené krystaly |
| Identifikace | |
| Registrační číslo CAS | 20644-87-5 |
| PubChem | 519800 |
| SMILES | O=C=(=C=O)(=C=O)(=C=O)(=C=O)=C=O |
| Vlastnosti | |
| Molární hmotnost | 219,00 g/mol |
| Teplota tání | rozklad |
| Hustota | 1,7 g/cm3 |
| Rozpustnost ve vodě | nerozpustný |
Některá data mohou pocházet z datové položky. | |
Hexakarbonyl vanadu, V(CO)6, je modrozelená těkavá pevná látka.[1] Tato sloučenina je z teoretického hlediska velmi zajímavá, protože jde o homoleptický karbonyl kovu, který je paramagnetický. Většina sloučenin se vzorcem Mx(CO)y dodržuje 18-elektronové pravidlo, ale V(CO)6 má 17 valenčních elektronů.
Příprava
Hexakarbonyl vanadu se připravuje redukcí chloridu vanaditého sodíkem v přítomnosti oxidu uhelnatého (160 °C, 20 MPa). Tato reakce se provádí zpravidla v diglymu:[1][2]
- 4 Na + VCl3 + 6 CO + 2 diglyme → + 3 NaCl
Produkt je poté redukován krystalickou kyselinou fosforečnou:
- V(CO) -
6 + 2 H3PO4 → 2 V(CO)6 + H2 + 2 H2PO -
4
Další možností je reduktivní karbonylace pomocí směsi zinku a hořčíku v nadbytku pyridinu při teplotě 120-140 °C.[3]
Struktura
V(CO)6 má oktaedrickou geometrii, je izostrukturní s hexakarbonyl chromem a hexakarbonyl molybdenem. RTG strukturní analýza ukázala, že molekula je mírně deformována, axiální vazby V-C mají délku 1,993(2) Å, zatímco čtyři ekvatoriální vazby V-C jsou mírně delší, 2,005(2) Å.[4]
Reakce
Hexakarbonyl vanadu je termicky nestabilní. Primární reakcí je redukce na anion V(CO) -
6 . Také lze provést substituci terciárními fosfiny, ta ale často vede k disproporcionaci.
Reakce se zdroji cyklopentadienylového aniontu vede ke vzniku oranžového komplexu (C5H5)V(CO)4. Ten se řadí do skupiny polosendvičových komplexů.[5]
Odkazy
Reference
V tomto článku byl použit překlad textu z článku Vanadium hexacarbonyl na anglické Wikipedii.
- ↑ a b GREENWOOD, Norman Neill. Chemie prvků. Sv. 1.. 1. vyd. vyd. Praha: Informatorium 793 s., 1 příl s. Dostupné online. ISBN 80-85427-38-9, ISBN 978-80-85427-38-7. OCLC 320245801 S. 1234.
- ↑ LIU, Xin; ELLIS, John E.; MESAROS, Eugen F. Transition Metal Carbonyl Compounds. Příprava vydání John R. Shapley. Hoboken, NJ, USA: John Wiley & Sons, Inc. Dostupné online. ISBN 978-0-471-64750-8, ISBN 978-0-471-65368-4. DOI 10.1002/0471653683.ch3. S. 96–132. DOI: 10.1002/0471653683.ch3.
- ↑ ERCOLI, R.; CALDERAZZO, F.; ALBEROLA, A. SYNTHESIS OF VANADIUM HEXACARBONYL. Journal of the American Chemical Society. 1960-06, roč. 82, čís. 11, s. 2966–2967. Dostupné online . ISSN 0002-7863. DOI 10.1021/ja01496a073. (anglicky)
- ↑ BELLARD, S.; RUBINSON, K. A.; SHELDRICK, G. M. Crystal and molecular structure of vanadium hexacarbonyl. Acta Crystallographica Section B Structural Crystallography and Crystal Chemistry. 1979-02-15, roč. 35, čís. 2, s. 271–274. Dostupné online . DOI 10.1107/S0567740879003332.
- ↑ WILFORD, J.B.; WHITLA, A.; POWELL, H.M. The crystal and molecular structure of π-cyclopentadienylvanadium tetracarbonyl. Journal of Organometallic Chemistry. 1967-06, roč. 8, čís. 3, s. 495–502. Dostupné online . DOI 10.1016/S0022-328X(00)83671-2. (anglicky)
Text je dostupný za podmienok Creative Commons Attribution/Share-Alike License 3.0 Unported; prípadne za ďalších podmienok. Podrobnejšie informácie nájdete na stránke Podmienky použitia.
Antény
Chemické zdroje elektriny
Chladenie v elektrotechnike
Elektrická sústava automobilu
Elektrická trakcia
Elektrické prístroje
Elektrické súčiastky
Elektrické spotrebiče
Elektrické stroje
Čítanie (elektrotechnika)
Činný výkon
Štatistická dynamika
Živý vodič
Admitancia
Antiparalelné zapojenie
Asynchrónny motor
Blúdivý prúd
Bočník (elektrotechnika)
Diak (polovodičový prvok)
Displej s kvapalnými kryštálmi
Elektrická inštalácia
Elektrická rezonancia
Elektrická sila
Elektrická vodivosť
Elektrické zariadenie
Elektrický obvod
Elektrický zvonec
Elektroenergetika
Elektromer
Elektrometer
Elektromobil
Elektromotor
Elektromotorické napätie
Elektrotechnický náučný slovník
Elektrotechnika
Elektrotechnológia
Fázor
Faradayova klietka
Frekvencia (fyzika)
Graetzov mostík
Impedancia
Indukčnosť
Induktancia
Istič
Izolácia (elektrotechnika)
Izolant
Jadro vodiča
Jednobran
Jednosmerný prúd
Joulovo teplo
Katóda
Koaxiálny kábel
Kompenzácia účinníka
Konduktometria
Konektor (elektrotechnika)
Korónový výboj
Lanko (elektrotechnika)
Leptanie
Logické hradlo
Magnetická susceptibilita
Magnetizácia (veličina)
Merný elektrický odpor
Mobilné zariadenie
Napájací zdroj
Napäťový chránič
Napäťový násobič
Nortonova veta
Odpínač
Odpojovač
OLED
Olovený akumulátor
Paralelné zapojenie
Peltierov článok
Plošná hustota elektrického prúdu
Poistka (elektrotechnika)
Posuvný prúd
Prúdový chránič
Prenosové médium
Prieletový klystrón
Primárny elektrochemický článok
Reaktancia
Rekuperácia (dopravný prostriedok)
Relé
Reproduktorová výhybka
Rezistancia
Rozhranie (interface)
Sériové zapojenie
Seebeckov jav
Sekundárny elektrochemický článok
Settopbox
Skrat
Sonar
Spínač
Spínaný zdroj
Straty v mikropásikových vedeniach
Striedavý prúd
Stupeň ochrany krytom
Svetelná výbojka
Symetrizačný člen
Technická normalizácia
Tepelné relé
Tepelne vodivostný detektor
Termočlánok
Théveninova veta
Transformátor
Transformátor s fázovou reguláciou
Trojfázová sústava
Tuhá fáza (elektronika)
Tyratrón
Usmerňovač (elektrotechnika)
Uzemnenie
Uzol (vodiče)
Vírivý prúd
Výbojka
Varistor
Ventilátor
Vodič (elektrotechnika)
Voltov stĺp
Vstavaný systém
Zásuvka (elektrotechnika)
Zdroj (elektrotechnika)
Zisk antény
Text je dostupný za podmienok Creative
Commons Attribution/Share-Alike License 3.0 Unported; prípadne za ďalších
podmienok.
Podrobnejšie informácie nájdete na stránke Podmienky
použitia.
www.astronomia.sk | www.biologia.sk | www.botanika.sk | www.dejiny.sk | www.economy.sk | www.elektrotechnika.sk | www.estetika.sk | www.farmakologia.sk | www.filozofia.sk | Fyzika | www.futurologia.sk | www.genetika.sk | www.chemia.sk | www.lingvistika.sk | www.politologia.sk | www.psychologia.sk | www.sexuologia.sk | www.sociologia.sk | www.veda.sk I www.zoologia.sk


