A | B | C | D | E | F | G | H | CH | I | J | K | L | M | N | O | P | Q | R | S | T | U | V | W | X | Y | Z | 0 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9
| Chlorid thiofosforylu | |
|---|---|
 Strukturní vzorec | |
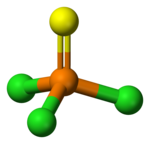 Model molekuly | |
| Obecné | |
| Systematický název | chlorid thiofosforylu |
| Ostatní názvy | thiofosforylchlorid, sulfochlorid fosforečný |
| Sumární vzorec | PSCl3 |
| Vzhled | bílé krystaly[1] |
| Identifikace | |
| Registrační číslo CAS | 3982-91-0 |
| EC-no (EINECS/ELINCS/NLP) | 223-622-6 |
| PubChem | 19883 |
| SMILES | P(=S)(Cl)(Cl)Cl |
| InChI | InChI=1S/Cl3PS/c1-4(2,3)5 |
| Vlastnosti | |
| Molární hmotnost | 169,40 g/mol |
| Teplota tání | −35 °C (238 K)[1] |
| Teplota varu | 125 °C (398 K)[1] |
| Hustota | 1,635 g/cm3[1] |
| Index lomu | 1,635[1] |
| Rozpustnost ve vodě | reaguje[1] |
| Rozpustnost v polárních rozpouštědlech | rozpustný v chloroformu[1] |
| Rozpustnost v nepolárních rozpouštědlech | rozpustný v benzenu, tetrachlormethanu a sirouhlíku[1] |
| Tlak páry | 2,9 kPa[1] |
| Bezpečnost | |
| [1] | |
| H-věty | H302 H314 H318 H335 H412[1] |
| P-věty | P260 P261 P264+265 P270 P271 P273 P280 P284 P301+317 P301+330+331 P302+361+354 P304+340 P305+354+338 P316 P317 P319 P320 P321 P330 P363 P403+233 P405 P501[1] |
Některá data mohou pocházet z datové položky. | |
Chlorid thiofosforylu je anorganická sloučenina se vzorcem PSCl3.[2] Jedná se o bezbarvou, na vzduchu dýmající kapalinu. Používá se na thiofosforylace organických sloučenin, například při výrobě insekticidů.
Příprava a výroba
Chlorid thiofosforylu lze z chloridu fosforitého získat několika způsoby. V průmyslu se používá oxidace nadbytkem síry při teplotě 180 °C.[3]
- PCl3 + S → PSCl3
S pomocí katalyzátorů lze reakci provést i za nižších teplot. Přečišťování se provádí destilací.
Další možností je reakce sulfidu a chloridu fosforečného.[4]
- 3 PCl5 + P2S5 → 5 PSCl3
Struktura
Chlorid thiofosforylu je tetraedrický a má molekulovou symetrii C3v. Délka vazby P=S je 189 pm a u vazby P–Cl činí 201 pm; úhel vazby Cl-P-Cl má velikost 102°.[5]
Reakce
PSCl3 se rozpouští v benzenu, tetrachlormethanu, chloroformu, a sulfidu uhličitém.[2] V zásaditých roztocích a sloučeninách obsahující hydroxylové skupiny, jako jsou alkoholy, se hydrolyzuje za vzniku thiofosforečnanů.[3] S vodou tato látka reaguje, přičemž produkty se liší podle reakčních podmínek; může jít o kyselinu fosforečnou, sulfan a kyselinu chlorovodíkovou, nebo kyselinu dichlorthiofosforečnou a chlorovodíkovou.[6]
- PSCl3 + 4 H2O → H3PO4 + H2S + 3 HCl PSCl3 + H2O → HO-P(=S)Cl2 + HCl
PSCl3 se používá k navazování thiofosforylových skupin, P=S, na organické sloučeniny.[3] Tyto přeměny lze provést u aminů a alkoholů, a to i aminoalkoholů, diolů, a diaminů.[2] V průmyslu se chlorid tthiofosforylu používá na výrobu insekticidů, jako je například parathion.[6]
- PSCl3 + 2 CH3CH2OH → (CH3CH2-O-)2P(=S)-Cl + 2 HCl
- (CH3CH2-O-)2P(=S)-Cl + Na+ → (CH3CH2-O-)2P(=S)-O-C6H4-NO2 + NaCl
PSCl3 reaguje s terciárními amidy, přičemž se vytváří thioamidy.[2]:
- C6H5-C(=O)-N(-CH3)2 + PSCl3 → C6H5-C(=S)-N(-CH3)2 + POCl3
S methylmagnesiumjodidem vytváří tetramethyldifosfindisulfid, (H3C-)2P(=S)-P(=S)(-CH3)2.[7]
Reference
V tomto článku byl použit překlad textu z článku Thiophosphoryl chloride na anglické Wikipedii.
- ↑ a b c d e f g h i j k l https://pubchem.ncbi.nlm.nih.gov/compound/19883
- ↑ a b c d Spilling, C. D. Thiophosphoryl Chloride, Encyclopedia of Reagents for Organic Synthesis John Wiley & Sons, Weinheim, 2001 DOI: 10.1002/047084289X.rt104
- ↑ a b c G. Betterman; W. Krause; G. Riess; T. Hofmann. Ullmann’s Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH, 2005. ISBN 3527306730. DOI 10.1002/14356007.a19_527. Kapitola Phosphorus Compounds, Inorganic.
- ↑ Martin, D. R.; Duvall, W. M. “Phosphorus(V) Sulfochloride” Inorganic Syntheses, 1953, p73 DOI:10.1002/9780470132357.ch24
- ↑ Kuchitsu Kozo; Tohei Moritani; Yonezo Morino. Molecular structures of phosphoryl fluoride, phosphoryl chloride, and thiophosphoryl chloride studied by gas electron diffraction. Inorganic Chemistry. 1971, s. 344–350. DOI 10.1021/ic50096a025.
- ↑ a b Fee, D. C.; Gard, D. R.; Yang, C. “Phosphorus Compounds” Kirk-Othmer Encyclopedia of Chemical Technology John Wiley & Sons: New York, 2005 DOI:10.1002/0471238961.16081519060505.a01.pub2
- ↑ G. W. Parshall "Tetramethylbiphosphine Disulfide" Organic Syntheses 1965, volume 45, p. 102 DOI:10.15227/orgsyn.045.0102
Text je dostupný za podmienok Creative Commons Attribution/Share-Alike License 3.0 Unported; prípadne za ďalších podmienok. Podrobnejšie informácie nájdete na stránke Podmienky použitia.
Antény
Chemické zdroje elektriny
Chladenie v elektrotechnike
Elektrická sústava automobilu
Elektrická trakcia
Elektrické prístroje
Elektrické súčiastky
Elektrické spotrebiče
Elektrické stroje
Čítanie (elektrotechnika)
Činný výkon
Štatistická dynamika
Živý vodič
Admitancia
Antiparalelné zapojenie
Asynchrónny motor
Blúdivý prúd
Bočník (elektrotechnika)
Diak (polovodičový prvok)
Displej s kvapalnými kryštálmi
Elektrická inštalácia
Elektrická rezonancia
Elektrická sila
Elektrická vodivosť
Elektrické zariadenie
Elektrický obvod
Elektrický zvonec
Elektroenergetika
Elektromer
Elektrometer
Elektromobil
Elektromotor
Elektromotorické napätie
Elektrotechnický náučný slovník
Elektrotechnika
Elektrotechnológia
Fázor
Faradayova klietka
Frekvencia (fyzika)
Graetzov mostík
Impedancia
Indukčnosť
Induktancia
Istič
Izolácia (elektrotechnika)
Izolant
Jadro vodiča
Jednobran
Jednosmerný prúd
Joulovo teplo
Katóda
Koaxiálny kábel
Kompenzácia účinníka
Konduktometria
Konektor (elektrotechnika)
Korónový výboj
Lanko (elektrotechnika)
Leptanie
Logické hradlo
Magnetická susceptibilita
Magnetizácia (veličina)
Merný elektrický odpor
Mobilné zariadenie
Napájací zdroj
Napäťový chránič
Napäťový násobič
Nortonova veta
Odpínač
Odpojovač
OLED
Olovený akumulátor
Paralelné zapojenie
Peltierov článok
Plošná hustota elektrického prúdu
Poistka (elektrotechnika)
Posuvný prúd
Prúdový chránič
Prenosové médium
Prieletový klystrón
Primárny elektrochemický článok
Reaktancia
Rekuperácia (dopravný prostriedok)
Relé
Reproduktorová výhybka
Rezistancia
Rozhranie (interface)
Sériové zapojenie
Seebeckov jav
Sekundárny elektrochemický článok
Settopbox
Skrat
Sonar
Spínač
Spínaný zdroj
Straty v mikropásikových vedeniach
Striedavý prúd
Stupeň ochrany krytom
Svetelná výbojka
Symetrizačný člen
Technická normalizácia
Tepelné relé
Tepelne vodivostný detektor
Termočlánok
Théveninova veta
Transformátor
Transformátor s fázovou reguláciou
Trojfázová sústava
Tuhá fáza (elektronika)
Tyratrón
Usmerňovač (elektrotechnika)
Uzemnenie
Uzol (vodiče)
Vírivý prúd
Výbojka
Varistor
Ventilátor
Vodič (elektrotechnika)
Voltov stĺp
Vstavaný systém
Zásuvka (elektrotechnika)
Zdroj (elektrotechnika)
Zisk antény
Text je dostupný za podmienok Creative
Commons Attribution/Share-Alike License 3.0 Unported; prípadne za ďalších
podmienok.
Podrobnejšie informácie nájdete na stránke Podmienky
použitia.
www.astronomia.sk | www.biologia.sk | www.botanika.sk | www.dejiny.sk | www.economy.sk | www.elektrotechnika.sk | www.estetika.sk | www.farmakologia.sk | www.filozofia.sk | Fyzika | www.futurologia.sk | www.genetika.sk | www.chemia.sk | www.lingvistika.sk | www.politologia.sk | www.psychologia.sk | www.sexuologia.sk | www.sociologia.sk | www.veda.sk I www.zoologia.sk





