A | B | C | D | E | F | G | H | CH | I | J | K | L | M | N | O | P | Q | R | S | T | U | V | W | X | Y | Z | 0 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9
| Acetylaceton | |
|---|---|
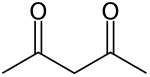 strukturní vzorec | |
 model molekuly (enolforma) | |
 model molekuly (ketoforma) | |
| Obecné | |
| Systematický název | pentan-2,4-dion |
| Anglický název | acetylacetone |
| Německý název | Acetylaceton |
| Funkční vzorec | CH3COCH2COCH3 (keto forma) |
| Sumární vzorec | C5H8O2 |
| Vzhled | bezbarvá kapalina |
| Identifikace | |
| Registrační číslo CAS | 123-54-6 |
| SMILES | O=C(C)CC(=O)C CC(=O)CC(=O)C |
| InChI | InChI=1S/C5H8O2/c1-4(6)3-5(2)7/h3H2,1-2H3 |
| Vlastnosti | |
| Molární hmotnost | 100,12 g/mol |
| Teplota tání | -23 °C (250 K) |
| Teplota varu | 140 °C (413 K) |
| Hustota | 0,975 g/cm3 |
| Rozpustnost ve vodě | 16 g/100 ml |
| Měrná magnetická susceptibilita | 5,48×105 μm3/g |
| Bezpečnost | |
| [1] | |
| R-věty | R10 R22 |
| S-věty | S2 S21 S23 S24/25 |
| Teplota vzplanutí | 34 °C |
| Teplota vznícení | 340 °C |
| Meze výbušnosti | 2,4 %-11,6 % |
Acetylaceton (systematický název pentan-2,4-dion) je organická sloučenina, která vytváří dva tautomery. Ketoforma má vzorec CH3COCH2COCH3.
Přestože je sloučenina nazvána podle diketonové formy, enolová forma je významnou složkou látky[2] a v mnoha rozpouštědlech převažuje.
Tato látka je prekurzorem acetylacetonátu (acac), běžného bidentátního ligandu. Je také základem pro syntézu heterocyklických sloučenin.
Vlastnosti
Tautomerie
Keto- a enolforma existují společně; jedná se o tautomery. Enolforma má symetrii C2v, což znamená, že vodíkový atom je rovnoměrně sdílen mezi oběma kyslíkovými atomy.[3] V plynném skupenství je rovnovážná konstanta Kketo→enol 11,7 (ve prospěch enolformy). Oba tautomery se dají snadno rozlišit pomocí NMR spektroskopie, infračervené spektroskopie a dalších metod.[4][5]
| Rozpouštědlo | Kketo→enol |
|---|---|
| Plynné skupenství | 11,7 |
| Cyklohexan | 42 |
| Toluen | 10 |
| THF | 7,2 |
| DMSO | 2 |
| Voda | 0,23 |
Rovnovážná konstanta je vysoká v nepolárních rozpouštědlech; ketoforma má větší zastoupení v polárních rozpouštědlech s přítomností vodíkových vazeb, například ve vodě. [6]
Kyselost/zásaditost
Acetylaceton je slabá kyselina:
| rozpouštědlo | T/°C | pKa[7] |
|---|---|---|
| 40% ethanol/voda | 30 | 9,8 |
| 70% 1,4-dioxan/voda | 28 | 12,5 |
| 80% DMSO/voda | 25 | 10,16 |
| DMSO | 25 | 13,41 |
| voda | 25 | 8,99±0,04 |
Velmi silné zásady, například organolithné sloučeniny, způsobují dvojnásobnou deprotonaci acetylacetonu. Vzniklé produkty mohou být alkylovány.
Příprava a výroba
Acetylaceton se průmyslově vyrábí tepelným přesmykem isopropenylacetátu[8]: CH2=C(CH3)OC(O)CH3 → CH3C(O)CH2C(O)CH3
Metody laboratorní přípravy začínají acetonem. Prvním způsobem je reakce acetonu s acetanhydridem za přítomnosti BF3 jako katalyzátoru:
(CH3CO)2O + CH3C(O)CH3 → CH3C(O)CH2C(O)CH3
Druhý způsob spočívá v kondenzaci acetonu a ethylacetátu následované reakcí s kyselinou:
NaOEt + EtO2CCH3 + CH3C(O)CH3 → NaCH3C(O)CHC(O)CH3 + 2 EtOH
NaCH3C(O)CHC(O)CH3 + HCl → CH3C(O)CH2C(O)CH3 + NaCl
Díky jednoduchosti uvedených postupů je známo mnoho acetylacetonátů, tedy solí a esterů acetylacetonu, například C6H5C(O)CH2C(O)C6H5 (dbaH) a (CH3)3CC(O)CH2C(O)CC(CH3)3.
Reakce
Kondenzace
Acetylaceton je všestranným prekurzorem heterocyklických sloučenin, jelikož obě ketoskupiny mohou podstoupit kondenzační reakce. Reakcí s hydrazinem vznikají pyrazoly, s močovinou pyrimidiny.
Koordinační chemie
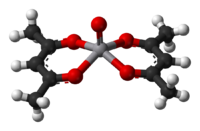
Acetylacetonátový aniont, acac-, vytváří komplexy s mnoha ionty přechodných kovů. Hlavním způsobem jejich přípravy je reakce příslušného iontu s acetylacetonem za přítomnosti zásady (B):
MBz + z Hacac ⇌ M(acac)z + z BH
Zásada umožňuje odstranění protonů z acetylacetonu a posouvá rovnováhu reakce ve prospěch komplexu. Oba kyslíkové atomy se naváží na kov za vzniku šestičlenného chelátového kruhu. V některých případech je chelatační efekt tak silný, že k tvorbě komplexu není třeba přítomnost zásady. Jelikož takový komplex nemá elektrický náboj, je nerozpustný ve vodě ale rozpustný v nepolárních organických rozpouštědlech.
Biologická rozložitelnost
Acetylaceton se rozkládá působením enzymu acetylacetondioxygenázy, který štěpí vazbu C-C v molekule za vzniku acetátu a 2-oxopropanalu. Enzym k činnosti potřebuje železnaté nebo zinečnaté kationty, které slouží jako prostetická skupina. Biologický rozklad acetylacetonu byl pozorován u bakterie Acinetobacter johnsonii.[9]
C5H8O2 + O2 → C2H4O2 + C3H4O2
Reference
V tomto článku byl použit překlad textu z článku Acetylacetone na anglické Wikipedii.
- ↑ Acetylacetone. pubchem.ncbi.nlm.nih.gov . PubChem . Dostupné online. (anglicky)
- ↑ O'BRIEN, Brian. Co(tfa)3 & Co(acac)3 handout . Gustavus Adolphus College. Dostupné online. (anglicky)
- ↑ CAMINATI, W.; GRABOW, J.-U. The C2v Structure of Enolic Acetylacetone. Journal of the American Chemical Society. 2006, roč. 128, čís. 3, s. 854–857. DOI 10.1021/ja055333g. PMID 16417375. (anglicky)
- ↑ MANBECK, Kimberly A.; BOAZ, Nicholas C.; BAIR, Nathaniel C.; SANDERS, Allix M. S. Substituent Effects on Keto–Enol Equilibria Using NMR Spectroscopy. Journal of Chemical Education. 2011, roč. 88, čís. 10, s. 1444–1445. DOI 10.1021/ed1010932. (anglicky)
- ↑ YOSHIDA, Z.; OGOSHI, H.; TOKUMITSU, T. Intramolecular hydrogen bond in enol form of 3-substituted-2,4-pentanedione. Tetrahedron. 1970, roč. 26, s. 5691–5697. DOI 10.1016/0040-4020(70)80005-9. (anglicky)
- ↑ REICHARDT, Christian. Solvents and Solvent Effects in Organic Chemistry. : Wiley-VCH, 2003. ISBN 3-527-30618-8.
- ↑ IUPAC SC-Database A comprehensive database of published data on equilibrium constants of metal complexes and ligands
- ↑ SIEGEL, Hardo; EGGERSDORFER, Manfred. Ullmann's Encyclopedia of Industrial Chemistry. Ketones. Weinheim: Wiley-VCH, 2002. DOI 10.1002/14356007.a15_077.
- ↑ STRAGANZ, G.D.; GLIEDER, A.; BRECKER, L.; RIBBONS, D.W. Acetylacetone-cleaving enzyme Dke1: a novel C–C-bond-cleaving enzyme from Acinetobacter johnsonii. Biochem. J.. 2003, roč. 369, čís. 3, s. 573–581. DOI 10.1042/BJ20021047. PMID 12379146. (anglicky)
Text je dostupný za podmienok Creative Commons Attribution/Share-Alike License 3.0 Unported; prípadne za ďalších podmienok. Podrobnejšie informácie nájdete na stránke Podmienky použitia.
Antény
Chemické zdroje elektriny
Chladenie v elektrotechnike
Elektrická sústava automobilu
Elektrická trakcia
Elektrické prístroje
Elektrické súčiastky
Elektrické spotrebiče
Elektrické stroje
Čítanie (elektrotechnika)
Činný výkon
Štatistická dynamika
Živý vodič
Admitancia
Antiparalelné zapojenie
Asynchrónny motor
Blúdivý prúd
Bočník (elektrotechnika)
Diak (polovodičový prvok)
Displej s kvapalnými kryštálmi
Elektrická inštalácia
Elektrická rezonancia
Elektrická sila
Elektrická vodivosť
Elektrické zariadenie
Elektrický obvod
Elektrický zvonec
Elektroenergetika
Elektromer
Elektrometer
Elektromobil
Elektromotor
Elektromotorické napätie
Elektrotechnický náučný slovník
Elektrotechnika
Elektrotechnológia
Fázor
Faradayova klietka
Frekvencia (fyzika)
Graetzov mostík
Impedancia
Indukčnosť
Induktancia
Istič
Izolácia (elektrotechnika)
Izolant
Jadro vodiča
Jednobran
Jednosmerný prúd
Joulovo teplo
Katóda
Koaxiálny kábel
Kompenzácia účinníka
Konduktometria
Konektor (elektrotechnika)
Korónový výboj
Lanko (elektrotechnika)
Leptanie
Logické hradlo
Magnetická susceptibilita
Magnetizácia (veličina)
Merný elektrický odpor
Mobilné zariadenie
Napájací zdroj
Napäťový chránič
Napäťový násobič
Nortonova veta
Odpínač
Odpojovač
OLED
Olovený akumulátor
Paralelné zapojenie
Peltierov článok
Plošná hustota elektrického prúdu
Poistka (elektrotechnika)
Posuvný prúd
Prúdový chránič
Prenosové médium
Prieletový klystrón
Primárny elektrochemický článok
Reaktancia
Rekuperácia (dopravný prostriedok)
Relé
Reproduktorová výhybka
Rezistancia
Rozhranie (interface)
Sériové zapojenie
Seebeckov jav
Sekundárny elektrochemický článok
Settopbox
Skrat
Sonar
Spínač
Spínaný zdroj
Straty v mikropásikových vedeniach
Striedavý prúd
Stupeň ochrany krytom
Svetelná výbojka
Symetrizačný člen
Technická normalizácia
Tepelné relé
Tepelne vodivostný detektor
Termočlánok
Théveninova veta
Transformátor
Transformátor s fázovou reguláciou
Trojfázová sústava
Tuhá fáza (elektronika)
Tyratrón
Usmerňovač (elektrotechnika)
Uzemnenie
Uzol (vodiče)
Vírivý prúd
Výbojka
Varistor
Ventilátor
Vodič (elektrotechnika)
Voltov stĺp
Vstavaný systém
Zásuvka (elektrotechnika)
Zdroj (elektrotechnika)
Zisk antény
Text je dostupný za podmienok Creative
Commons Attribution/Share-Alike License 3.0 Unported; prípadne za ďalších
podmienok.
Podrobnejšie informácie nájdete na stránke Podmienky
použitia.
www.astronomia.sk | www.biologia.sk | www.botanika.sk | www.dejiny.sk | www.economy.sk | www.elektrotechnika.sk | www.estetika.sk | www.farmakologia.sk | www.filozofia.sk | Fyzika | www.futurologia.sk | www.genetika.sk | www.chemia.sk | www.lingvistika.sk | www.politologia.sk | www.psychologia.sk | www.sexuologia.sk | www.sociologia.sk | www.veda.sk I www.zoologia.sk