A | B | C | D | E | F | G | H | CH | I | J | K | L | M | N | O | P | Q | R | S | T | U | V | W | X | Y | Z | 0 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9
| Pyrylium | |
|---|---|
 Strukturní vzorec | |
| Obecné | |
| Systematický název | pyrylium |
| Ostatní názvy | pyranium |
| Sumární vzorec | C5H5O+ |
| Identifikace | |
| Registrační číslo CAS | 289-67-8 |
| PubChem | 9548819 |
| ChEBI | 36120 |
| SMILES | 1ccccc1 |
| InChI | InChI=1/C5H5O/c1-2-4-6-5-3-1/h1-5H/q+1 |
| Vlastnosti | |
| Molární hmotnost | 81,092 g/mol |
Některá data mohou pocházet z datové položky. | |
Pyrylium je kation se vzorcem C5H5O+, skládající se z šestičlenného cyklu tvořeného pěti atomy uhlíku, kde je na každý navázán jeden vodík, a jeden kladně nabitý trojvazný atom kyslíku. Vazby v uzavřeném řetězci vytvářejí konjugovaný systém, podobný jako u benzenu, čímž se ion stává aromatickým. Pyrilium patří mezi oniové ionty.
Soli
Pyrylium a jeho deriváty tvoří stabilní soli s mnoha různými anionty.[1][2][3][4][5]
Chloristan pyrylia je rozpustný v acetonitrilu.
Chloristan trimethylpyrylia má teplotu tání 246-247 °C.
Tetrafluorboritan 2,4,6-trifenylpyrylia je žlutá pevná látka tající při 214 až 215 °C.
Stejné zbarvení vykazuje též chlorid 2-methyl-4,6-difenylpyryla, jenž má teplotu tání 125 až 126 °C.
Deriváty
Mnoho významných kationtů je odvozeno od pyrylia nahrazením jednoho či více vodíkových atomů organickými funkčními skupinami. 2,4,6-trifenylpyrilium, nazývané také jako Katritzkého sůl, je součástí katalyzátorů řady překřížených párovacích reakcí.[6]
Chemické vlastnosti
Podobně jako jiné oniové ionty je pyrylium v neutrálních vodných roztocích nestálé. Vyznačuje se ovšem výrazně nižší reaktivitou než běžné oxoniové ionty, což způsobuje aromatická stabilizace. 2,4,6-trifenylpyrylium často reaguje s alifatickými aminy za vzniku pyridiniových solí, čímž aminy aktivuje vůči oxidačním adičním reakcím s komplexy kovů, jako je nikl.[7]
Pyryliové kationty rovněž vstupují do reakcí s nukleofily v pozicích 2, 4, a 6, čímž spouštějí řadu dalších reakcí. Vysoká elektronegativita kyslíku způsobuje silné narušení cyklického řetězce.
Příprava
Pyryliové soli lze snadno připravit kondenzačními reakcemi.
Soli obsahující aromatické substituenty, například tetrafluorboritan 2,4,6-trifenylpyrylia, je možné získat reakcemi dvou ekvivalentů acetofenonu s jedním ekvivalentem benzaldehydu za přítomnosti kyseliny tetrafluorborité a oxidačního činidla (tento postup se nazývá Diltheyova syntéza). Pyryliové soli s alkylovými skupinami, například ty odvozené od 2,4,6-trimethylpyrylia, se nejsnadněji připravují Balabanovou-Nenitzescuovou-Praillovou syntézou z terc-butanolu a acetanhydridu za přítomnosti kyseliny tetrafluorborité, chloristé nebo trifluormethansulfonové.[8][9] 2,4,6-trifenylpyryliové soli mohou být zásadami přeměněny na stabilní 1,5-endiony, ovšem obdobné produkty reakcí 2,4,6-trimethylpyryliových solí v horkých roztocích alkalických hydroxidů jsou nestabilní a dále se přeměňují vnitromolekulárními kondenzacemi na 3,5-dimethylfenoly. V teplé těžké vodě probíhá u 2,4,6-trimethylpyryliových solí izotopová výměna 4-methylových vodíků rychleji než na pozicích 2- a 6-, což dovoluje regioselektivně připravovat deuterované sloučeniny.
Reakce pyryliových solí s nukleofily z nich činí vhodné prekurzory dalších látek, které jsou více aromatické. Reakcemi s amoniakem vznikají pyridiny,[10] s primárními aminy pyridiniové soli, s hydroxylaminem pyridin-N-oxidy, s fosfiny fosforiny. Se sulfanem tvoří thiopyryliové soli a za přítomnosti acetonitrilu či nitromethanu dávají pyriliové soli deriváty benzenu.
Pyrony
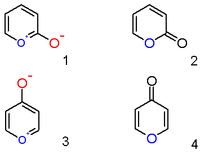
Pyriliový kation s navázaným hydroxylovým aniontem v pozici 2 není zwitteriontovou organickou sloučeninou (1), nýbrž neutrálním nenasyceným laktonem nebo 2-pyronem (pyran-2-onem) (2). Významnými zástupci této skupiny sloučenin jsou lumariny.
Obdobně jsou 4-hydroxylpyryliové sloučeniny 4-pyrony (pyran-4-ony) (4); sem patří například maltol.
Chemické vlastnosti

2-pyrony reagují s alkyny v Dielsových–Alderových reakcích za tvorby arenů a odštěpení oxidu uhličitého:[11]
Polycyklické pyryliové ionty
Chromenyliové ionty
Jeden bicyklický pyryliový ion se nazývá benzopyrylium (systematicky chromenylium), vzorec má C9H7O+. Lze ji považovat za nabitý derivát 2H-1-benzopyranu (2H-chromenu, C9H8O), nebo za nabitý substituovaný heterocyklický derivát naftalenu C10H8).
Flavyliové ionty
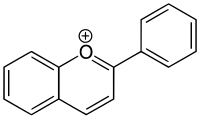
V biologii se 2-fenylbenzopyryliový ion často nazývá flavylium. Ke sloučeninám odvozeným od tohoto iontu patří antokyanidiny a antokyaniny, barviva vytvářející barvy mnoha květů.
Naftoxanthenový kation
Existují i vyšší polycyklické deriváty pyrylia, například naftoxantheniový kation. Jedná se o barvivo, které je velmi stabilní a jeho molekuly jsou aromatické. Absorbuje v oblasti ultrafialového záření a modrého světla a má neobvyklé fotofyzikální vlastnosti. Může být připraven chemickými nebo fotochemickými reakcemi.[12]
-
Benzopyryliumchlorid (chromenyliumchlorid), sůl chromenylia s chloridovým aniontem
-
Flavyliový kation
-
Naftoxanteniový kation
Odkazy
Související články
- Šestičlenné aromatické kruhy s jedním atomem uhlíku nahrazeným jinou skupinou: borabenzen, silabenzen, germabenzen, stannabenzen, pyridin, fosforin, arsabenzen, stibabenzen, bismabenzen, pyrylium, thiopyrylium, selenopyrylium, telluropyrylium
Externí odkazy
 Obrázky, zvuky či videa k tématu Pyryliové soli na Wikimedia Commons
Obrázky, zvuky či videa k tématu Pyryliové soli na Wikimedia Commons
Reference
V tomto článku byl použit překlad textu z článku Pyrylium salt na anglické Wikipedii.
- ↑ T. L. Gilchrist. Heterocyclic Chemistry. : ISBN 0-582-27843-0.
- ↑ A. T. Balaban; W. Schroth; G. Fischer. Pyrylium Salts. I. Synthesis. Advances in Heterocyclic Chemistry. 1969. DOI 10.1016/S0065-2725(08)60499-7.
- ↑ A. T. Balaban. New Trends in Heterocyclic Chemistry. : Elsevier, 1979. Dostupné online. ISBN 978-0-444-41737-4. Kapitola The Pyrylium Cation as a Synthon in Organic Chemistry, s. 79–111.
- ↑ A. T. Balaban. Organic Synthesis: Modern Trends. : Blackwell, 1987. Dostupné online. ISBN 0-632-02014-8. Kapitola Pyrylium Salts as Useful Synthons, s. 263–274.
- ↑ T. S. Balaban; A. T. Balaban. Hetarenes and Related Ring Systems, Six-membered Hetarenes with one Chalcogen. Stuttgart: Georg Thieme Verlag, 2003. ISBN 978-3-13-118641-6. Kapitola Pyrylium Salts, s. 11–200.
- ↑ A. T. Balaban; V. Wray. 13C n.m.r. spectra of some pyrylium salts and related compounds. Organic Magnetic Resonance. 1977. DOI 10.1002/mrc.1270090105.
- ↑ Yue Pang; Daniel Moser; Josep Cornella. Pyrylium Salts: Selective Reagents for the Activation of Primary Amino Groups in Organic Synthesis. Synthesis. 2020, s. 489. Dostupné online. DOI 10.1002/mrc.1270090105.
- ↑ BALABAN, A. T.; BOULTON, A. J. 2,4,6-Trimethyl-Pyrylium Tetrafluoroborate. Org. Synth.. 1973. Dostupné online.; Coll. Vol.. S. 1112–1113.
- ↑ BALABAN, A. T.; BOULTON, A. J. 2,4,6-Trimethyl-Pyrylium Trifluoromethanesulfonate. Org. Synth.. 1973. Dostupné online.; Coll. Vol.. S. 1114–1116.
- ↑ ANDERSON, A. G.; STANG, P. J. 2,6-Di-tert-Butyl-4-Methylpyridine. Org. Synth.. 1981, s. 34. Dostupné online.; Coll. Vol.. S. 144.
- ↑ P. M. Delaney; J. E. Moore; J. P. A. Harrity. An Alkynylboronic Ester Cycloaddition Route to Functionalised Aromatic Boronic Esters. Chemical Communications. 2006, s. 3323–3325. DOI 10.1039/b607322k.
- ↑ G. Bucher; R. Bresolí-Obach; C. Brosa; C. Flors; J. L. Luis; T. A. Grillo; S. Nonell. β-Phenyl quenching of 9-phenylphenalenones: a novel photocyclisation reaction with biological implications. Physical Chemistry Chemical Physics. 2014, s. 18813–18820. DOI 10.1039/C4CP02783C. Bibcode 2014PCCP...1618813B.
Text je dostupný za podmienok Creative Commons Attribution/Share-Alike License 3.0 Unported; prípadne za ďalších podmienok. Podrobnejšie informácie nájdete na stránke Podmienky použitia.
Antény
Chemické zdroje elektriny
Chladenie v elektrotechnike
Elektrická sústava automobilu
Elektrická trakcia
Elektrické prístroje
Elektrické súčiastky
Elektrické spotrebiče
Elektrické stroje
Čítanie (elektrotechnika)
Činný výkon
Štatistická dynamika
Živý vodič
Admitancia
Antiparalelné zapojenie
Asynchrónny motor
Blúdivý prúd
Bočník (elektrotechnika)
Diak (polovodičový prvok)
Displej s kvapalnými kryštálmi
Elektrická inštalácia
Elektrická rezonancia
Elektrická sila
Elektrická vodivosť
Elektrické zariadenie
Elektrický obvod
Elektrický zvonec
Elektroenergetika
Elektromer
Elektrometer
Elektromobil
Elektromotor
Elektromotorické napätie
Elektrotechnický náučný slovník
Elektrotechnika
Elektrotechnológia
Fázor
Faradayova klietka
Frekvencia (fyzika)
Graetzov mostík
Impedancia
Indukčnosť
Induktancia
Istič
Izolácia (elektrotechnika)
Izolant
Jadro vodiča
Jednobran
Jednosmerný prúd
Joulovo teplo
Katóda
Koaxiálny kábel
Kompenzácia účinníka
Konduktometria
Konektor (elektrotechnika)
Korónový výboj
Lanko (elektrotechnika)
Leptanie
Logické hradlo
Magnetická susceptibilita
Magnetizácia (veličina)
Merný elektrický odpor
Mobilné zariadenie
Napájací zdroj
Napäťový chránič
Napäťový násobič
Nortonova veta
Odpínač
Odpojovač
OLED
Olovený akumulátor
Paralelné zapojenie
Peltierov článok
Plošná hustota elektrického prúdu
Poistka (elektrotechnika)
Posuvný prúd
Prúdový chránič
Prenosové médium
Prieletový klystrón
Primárny elektrochemický článok
Reaktancia
Rekuperácia (dopravný prostriedok)
Relé
Reproduktorová výhybka
Rezistancia
Rozhranie (interface)
Sériové zapojenie
Seebeckov jav
Sekundárny elektrochemický článok
Settopbox
Skrat
Sonar
Spínač
Spínaný zdroj
Straty v mikropásikových vedeniach
Striedavý prúd
Stupeň ochrany krytom
Svetelná výbojka
Symetrizačný člen
Technická normalizácia
Tepelné relé
Tepelne vodivostný detektor
Termočlánok
Théveninova veta
Transformátor
Transformátor s fázovou reguláciou
Trojfázová sústava
Tuhá fáza (elektronika)
Tyratrón
Usmerňovač (elektrotechnika)
Uzemnenie
Uzol (vodiče)
Vírivý prúd
Výbojka
Varistor
Ventilátor
Vodič (elektrotechnika)
Voltov stĺp
Vstavaný systém
Zásuvka (elektrotechnika)
Zdroj (elektrotechnika)
Zisk antény
Text je dostupný za podmienok Creative
Commons Attribution/Share-Alike License 3.0 Unported; prípadne za ďalších
podmienok.
Podrobnejšie informácie nájdete na stránke Podmienky
použitia.
www.astronomia.sk | www.biologia.sk | www.botanika.sk | www.dejiny.sk | www.economy.sk | www.elektrotechnika.sk | www.estetika.sk | www.farmakologia.sk | www.filozofia.sk | Fyzika | www.futurologia.sk | www.genetika.sk | www.chemia.sk | www.lingvistika.sk | www.politologia.sk | www.psychologia.sk | www.sexuologia.sk | www.sociologia.sk | www.veda.sk I www.zoologia.sk