A | B | C | D | E | F | G | H | CH | I | J | K | L | M | N | O | P | Q | R | S | T | U | V | W | X | Y | Z | 0 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9
| Chlorid měďný | |
|---|---|
 | |
| Obecné | |
| Systematický název | Chlorid měďný |
| Anglický název | Copper(I) chloride |
| Německý název | Kupfer(I)-chlorid |
| Sumární vzorec | CuCl |
| Vzhled | bílý prášek |
| Identifikace | |
| Registrační číslo CAS | 7758-89-6 |
| Číslo EC (enzymy) | 231-842-9 |
| PubChem | 62652 |
| ChEBI | 53472 |
| Číslo RTECS | GL6990000 |
| Vlastnosti | |
| Molární hmotnost | 98,999 g/mol |
| Teplota tání | 430 °C |
| Teplota varu | 1 212 °C |
| Hustota | 4,139 g/cm3 |
| Dynamický viskozitní koeficient | 2,54 cP (527 °C) 1,92 cP (607 °C) 1,44 cP (697 °C) |
| Index lomu | nD= 1,973 |
| Rozpustnost ve vodě | 1,25 g/100 g (25 °C) |
| Rozpustnost v polárních rozpouštědlech | kys. chlorovodíková roztoky amonných solí roztoky kyanidů |
| Součin rozpustnosti | 1,86×10−7 |
| Relativní permitivita εr | 10 (20 °C) |
| Měrná magnetická susceptibilita | −5,026×10−6 cm3g−1 |
| Povrchové napětí | 92 mN/m (450 °C) |
| Struktura | |
| Krystalová struktura | krychlová |
| Hrana krystalové mřížky | a=545,7 pm |
| Dipólový moment | 4,27×10−30 Cm |
| Termodynamické vlastnosti | |
| Standardní slučovací entalpie ΔHf° | −136,5 kJ/mol |
| Entalpie tání ΔHt | 103,5 J/g |
| Entalpie varu ΔHv | 219,2 J/g |
| Standardní molární entropie S° | 87,1 JK−1 mol−1 |
| Standardní slučovací Gibbsova energie ΔGf° | −114,06 kJ/mol |
| Izobarické měrné teplo cp | 0,489 9 JK−1 g−1 |
| Bezpečnost | |
| [1] Varování[1] | |
| R-věty | R22, R50/53 |
| S-věty | (S2), S22, S60, S61 |
| NFPA 704 |  0
3
0
|
Některá data mohou pocházet z datové položky. | |
Chlorid měďný je anorganická sloučenina se vzorcem CuCl, binární chlorid mědi v nejnižším oxidačním čísle. Jedná se o bílou tuhou látku špatně rozpustnou ve vodě, avšak dobře rozpustnou v koncentrované kyselině chlorovodíkové. Nečisté vzorky jsou nazelenalé díky přítomnosti zeleného chloridu měďnatého.[2]
Vlastnosti

Chlorid měďný je Lewisovou kyselinou, klasifikovanou podle konceptu HSAB jako „měkkou“. Proto má tendenci tvořit stabilní komplexy s měkkými Lewisovými zásadami, například trifenylfosfinem:
- CuCl + P(C6H5)3 → 4
Přestože se CuCl příliš nerozpouští ve vodě, rozpouští se ve vodných roztocích obsahujících vhodné donorové molekuly. Tvoří komplexy s halogenidovými ionty, například s koncentrovanou kyselinou chlorovodíkovou tvoří H3O+ CuCl2−. Podobně tvoří komplexy také s CN−, S2O32− a NH3.
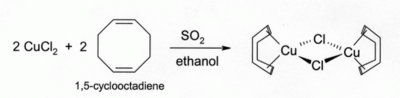
Roztoky CuCl s HCl nebo NH3 pohlcují oxid uhelnatý za vzniku bezbarvých komplexů, například dimeru s chloridovým můstkem 2. Stejný roztok s HCl reaguje také s acetylenem na . Roztok s amoniakem dává s acetylenem výbušný acetylid měďný. Komplexy CuCl s alkeny lze připravit redukcí CuCl2 oxidem siřičitým za přítomnosti alkenu v alkoholovém roztoku. Komplexy s dieny, například 1,5-cyklooktadienem, jsou zvláště stabilní:[3]
Za nepřítomnosti jiných ligandů jsou vodné roztoky CuCl nestabilní vzhledem k disproporcionaci na měď a chlorid měďnatý.[4] Částečně z tohoto důvodu se CuCl na vzduchu zbarvuje dozelena.
Použití
Hlavním použitím chloridu měďného je jako prekurzor pro výrobu fungicidního oxychloridu měďnatého. Pro tento účel se CuCl generuje synproporcionací a pak se oxiduje vzduchem:
- Cu + CuCl2 → 2 CuCl
- 6 CuCl + 3/2 O2 + 3 H2O → 2 Cu3Cl2(OH)4 + CuCl2
CuCl katalyzuje mnoho organických reakcí. Jeho afinity k oxidu uhelnatému v přítomnosti chloridu hlinitého se využívá v procesu COPureSM.
Organická syntéza
V Sandmeyerově reakci vede působení CuCl na arendiazoniové soli ke vzniku arylchloridů, například:[5]
Tato reakce má široký záběr a obvykle nabízí vysokou výtěžnost.
Polymery
CuCl se používá jako katalyzátor v radikálové polymerizaci přenosem atomu (ATRP).
Reference
V tomto článku byl použit překlad textu z článku Copper(I) chloride na anglické Wikipedii.
- ↑ a b Copper(I) chloride. pubchem.ncbi.nlm.nih.gov . PubChem . Dostupné online. (anglicky)
- ↑ United States Patent US4582579 "method of preparing cupric ion free cuprous chloride" Section 2, lines 4-41 , via www.freepatentsonline.com
- ↑ Nicholls, D. Complexes and First-Row Transition Elements, Macmillan Press, London, 1973.
- ↑ Greenwood, N.N.; Earnshaw, A. Chemistry of the Elements, 2nd ed., Butterworth-Heinemann, Oxford, UK, 1997.
- ↑ (a) Wade, L. G. Organic Chemistry, 5th ed., p. 871, Prentice Hall, Upper Saddle RIver, New Jersey, 2003. (b) March, J. Advanced Organic Chemistry, 4th ed., p. 723, Wiley, New York, 1992.
Literatura
- VOHLÍDAL, JIŘÍ; ŠTULÍK, KAREL; JULÁK, ALOIS. Chemické a analytické tabulky. 1. vyd. Praha: Grada Publishing, 1999. ISBN 80-7169-855-5.
- Mellor, J. W., A Comprehensive Treatise on Inorganic and Theoretical Chemistry, Volume III, pp157–168. Longmans, Green & Co., London, 1967 (new impression).
Externí odkazy
Text je dostupný za podmienok Creative Commons Attribution/Share-Alike License 3.0 Unported; prípadne za ďalších podmienok. Podrobnejšie informácie nájdete na stránke Podmienky použitia.
Antény
Chemické zdroje elektriny
Chladenie v elektrotechnike
Elektrická sústava automobilu
Elektrická trakcia
Elektrické prístroje
Elektrické súčiastky
Elektrické spotrebiče
Elektrické stroje
Čítanie (elektrotechnika)
Činný výkon
Štatistická dynamika
Živý vodič
Admitancia
Antiparalelné zapojenie
Asynchrónny motor
Blúdivý prúd
Bočník (elektrotechnika)
Diak (polovodičový prvok)
Displej s kvapalnými kryštálmi
Elektrická inštalácia
Elektrická rezonancia
Elektrická sila
Elektrická vodivosť
Elektrické zariadenie
Elektrický obvod
Elektrický zvonec
Elektroenergetika
Elektromer
Elektrometer
Elektromobil
Elektromotor
Elektromotorické napätie
Elektrotechnický náučný slovník
Elektrotechnika
Elektrotechnológia
Fázor
Faradayova klietka
Frekvencia (fyzika)
Graetzov mostík
Impedancia
Indukčnosť
Induktancia
Istič
Izolácia (elektrotechnika)
Izolant
Jadro vodiča
Jednobran
Jednosmerný prúd
Joulovo teplo
Katóda
Koaxiálny kábel
Kompenzácia účinníka
Konduktometria
Konektor (elektrotechnika)
Korónový výboj
Lanko (elektrotechnika)
Leptanie
Logické hradlo
Magnetická susceptibilita
Magnetizácia (veličina)
Merný elektrický odpor
Mobilné zariadenie
Napájací zdroj
Napäťový chránič
Napäťový násobič
Nortonova veta
Odpínač
Odpojovač
OLED
Olovený akumulátor
Paralelné zapojenie
Peltierov článok
Plošná hustota elektrického prúdu
Poistka (elektrotechnika)
Posuvný prúd
Prúdový chránič
Prenosové médium
Prieletový klystrón
Primárny elektrochemický článok
Reaktancia
Rekuperácia (dopravný prostriedok)
Relé
Reproduktorová výhybka
Rezistancia
Rozhranie (interface)
Sériové zapojenie
Seebeckov jav
Sekundárny elektrochemický článok
Settopbox
Skrat
Sonar
Spínač
Spínaný zdroj
Straty v mikropásikových vedeniach
Striedavý prúd
Stupeň ochrany krytom
Svetelná výbojka
Symetrizačný člen
Technická normalizácia
Tepelné relé
Tepelne vodivostný detektor
Termočlánok
Théveninova veta
Transformátor
Transformátor s fázovou reguláciou
Trojfázová sústava
Tuhá fáza (elektronika)
Tyratrón
Usmerňovač (elektrotechnika)
Uzemnenie
Uzol (vodiče)
Vírivý prúd
Výbojka
Varistor
Ventilátor
Vodič (elektrotechnika)
Voltov stĺp
Vstavaný systém
Zásuvka (elektrotechnika)
Zdroj (elektrotechnika)
Zisk antény
Text je dostupný za podmienok Creative
Commons Attribution/Share-Alike License 3.0 Unported; prípadne za ďalších
podmienok.
Podrobnejšie informácie nájdete na stránke Podmienky
použitia.
www.astronomia.sk | www.biologia.sk | www.botanika.sk | www.dejiny.sk | www.economy.sk | www.elektrotechnika.sk | www.estetika.sk | www.farmakologia.sk | www.filozofia.sk | Fyzika | www.futurologia.sk | www.genetika.sk | www.chemia.sk | www.lingvistika.sk | www.politologia.sk | www.psychologia.sk | www.sexuologia.sk | www.sociologia.sk | www.veda.sk I www.zoologia.sk