A | B | C | D | E | F | G | H | CH | I | J | K | L | M | N | O | P | Q | R | S | T | U | V | W | X | Y | Z | 0 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9
Halogenace je chemická reakce, kterou se zavádí halogen do molekuly organických sloučenin za vzniku halogenderivátů. Obecně to jsou všechny reakce, při kterých se vytváří vazba uhlík-halogen. Podle halogenu (fluor F2, chlor Cl2, brom Br2, jod I2) vstupujícího do reakce se halogenace detailněji nazývá fluorace, chlorace, bromace a jodace. Opačnou reakcí je dehalogenace, kdy je atom halogenu z molekuly odstraněn.
Halogenace probíhá především reakcí elementárních halogenů, solí halogenidů nebo halogenových kyselin s organickými sloučeninami. Nejvhodnějšími sloučeninami pro halogenaci jsou alkoholy, neboť jsou ze všech substrátů nejdostupnější.
Halogenderiváty
Výsledkem halogenace jsou halogenderiváty. Ty hrají významnou úlohu jako alkylační a arylační činidla při zavádění uhlíkatých řetězců do organických molekul, neboť halogenidové ionty se snadno oddělují. Z těchto důvodů obvykle halogenderiváty nepředstavují koncové produkty, ale meziprodukty pro další reakce. Například při reakci halogenu s alkenem dochází k rozštěpení π-vazby a vzniku halogenalkanu, který je reaktivnější než původní uhlovodík. Halogeny jsou pak dobrou odstupující skupinou v dalších reakcích, například nukleofilních alifatických substitucích a eliminačních reakcích.
Z technického hlediska je pro výrobu halogenderivátů důležitá dostupnost substrátu, jeho struktura nebo přítomnost dalších funkčních skupin, které by mohly reakci pozitivně ovlivnit. Řada halogenderivátů je v dnešní době vyráběna průmyslově, například nejrůznější polymery nebo léčiva.
Metody halogenace
Metody halogenace nebo také syntézy halogenderivátů jsou velmi rozmanité, nejdůležitější jsou dva typy reakcí:
- adiční reakce (AE, AR)
- substituční reakce (SN, SE, SR)
Adiční reakce
Adice halogenů na alkyny a alkeny
Adice halogenů na alkyny a alkeny je reakce, při níž vznikají halogenalkeny nebo halogenalkany. Například reakce alkynů s bromem probíhá ve dvou krocích:
V prvním kroku z bromu a ethynu vzniká dibromethen:

Ve druhém kroku z dibromethenu vzniká tetrabromethan:

Adice halogenovodíků na alkeny nebo alkyny
Adice halogenovodíků na alkeny nebo alkyny je reakcí, při které vznikají halogenalkeny nebo halogenalkany. Příkladem je adiční reakce kyseliny chlorovodíkové s butenem za vzniku chlorbutanu:
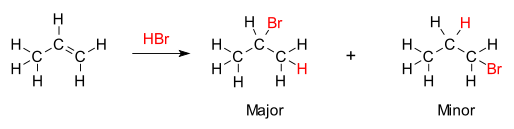
Adice halogenovodíků HX (X= F, Cl, Br, I) na alkyny a alkeny je jednou z nejstarších metod pro snadnost adice halogenovodíků na jednoduché alkeny. Její význam je však limitován nežádoucími vedlejšími reakcemi. Pro adiční reakci halogenovodíků s alkeny platí Markovnikovovo pravidlo:
Substituční reakce
Substituční halogenace alkanů
Halogenace alkanů probíhá jako radikálová substituce nebo přesněji radikálová halogenace. K tvorbě radikálů se nejčastěji využívá ultrafialové záření. Reakce obvykle probíhá u alkanů a alkylovaných arenů. Radikálovou halogenací se vyrábí například chloroform, dichlormethan a hexachlorbutadien. Příkladem radikálové halogenace je reakce chloru s methanem:
Substituční halogenace ketonů a aldehydů
Halogenace ketonů a aldehydů probíhá jako elektrofilní substituční reakce. Příkladem může být reakce obecného ketonu s bromem:
Substituční halogenace aromatických látek
Halogenace aromatických sloučenin probíhá jako elektrofilní aromatická substituce. Příkladem je chlorace benzenu. Chlor reaguje s benzenem za přítomnosti Lewisovy kyseliny a vzniká chlorbenzen a chlorovodík. Jako Lewisova kyselina se používá chlorid železitý nebo chlorid hlinitý. Tyto sloučeniny aktivují chlor, který by jinak s benzenem nereagoval. Reakce s bromem je analogická.
Další substituční halogenace
Pro zavedení halogenu do řetězce derivátů uhlovodíků se využívají například tyto reakce:
- nukleofilní substituce kyslíkaté skupiny v alkoholech, etherech a karboxylových kyselinách
- elektrofilní substituce v karbonylových sloučeninách a karboxylových kyselinách
Příklady halogenací
Jednoduchou halogenací je například příprava chloridu zlatitého chlorací zlata. Mezi specifičtější halogenační metody patří Hunsdieckerových reakce (z karboxylových kyselin) a Sandmeyerova reakce (arylhalogenidy).
Syntéza halothanu
Příkladem halogenace je organická syntéza anestetika halotanu z trichlorethylenu, která jako druhý krok zahrnuje bromaci při vysoké teplotě:[1]

Chlorace methanu
Chlorace methanu nebo také obecněji radikálová halogenace probíhá ve třech krocích:
1. Iniciace (zahájení, vznik radikálů)
- Cl2 → 2 Cl*
2. Propagace (šíření reakce)
- Cl* + CH4 → HCl + H3C*
- H3C* + Cl2 → CH3Cl + Cl*
3. Terminace (ukončení)
- 2 Cl* → Cl2
- Cl* + H3C* → CH3Cl
- H3C* + H3C* → CH3CH3
Reference
V tomto článku byly použity překlady textů z článků Halogenation na anglické Wikipedii a Halogenierung na německé Wikipedii.
- ↑ Synthesis of essential drugs, Ruben Vardanyan, Victor Hruby; Elsevier 2005 ISBN 0-444-52166-6
Externí odkazy
 Obrázky, zvuky či videa k tématu halogenace na Wikimedia Commons
Obrázky, zvuky či videa k tématu halogenace na Wikimedia Commons
Text je dostupný za podmienok Creative Commons Attribution/Share-Alike License 3.0 Unported; prípadne za ďalších podmienok. Podrobnejšie informácie nájdete na stránke Podmienky použitia.
Antény
Chemické zdroje elektriny
Chladenie v elektrotechnike
Elektrická sústava automobilu
Elektrická trakcia
Elektrické prístroje
Elektrické súčiastky
Elektrické spotrebiče
Elektrické stroje
Čítanie (elektrotechnika)
Činný výkon
Štatistická dynamika
Živý vodič
Admitancia
Antiparalelné zapojenie
Asynchrónny motor
Blúdivý prúd
Bočník (elektrotechnika)
Diak (polovodičový prvok)
Displej s kvapalnými kryštálmi
Elektrická inštalácia
Elektrická rezonancia
Elektrická sila
Elektrická vodivosť
Elektrické zariadenie
Elektrický obvod
Elektrický zvonec
Elektroenergetika
Elektromer
Elektrometer
Elektromobil
Elektromotor
Elektromotorické napätie
Elektrotechnický náučný slovník
Elektrotechnika
Elektrotechnológia
Fázor
Faradayova klietka
Frekvencia (fyzika)
Graetzov mostík
Impedancia
Indukčnosť
Induktancia
Istič
Izolácia (elektrotechnika)
Izolant
Jadro vodiča
Jednobran
Jednosmerný prúd
Joulovo teplo
Katóda
Koaxiálny kábel
Kompenzácia účinníka
Konduktometria
Konektor (elektrotechnika)
Korónový výboj
Lanko (elektrotechnika)
Leptanie
Logické hradlo
Magnetická susceptibilita
Magnetizácia (veličina)
Merný elektrický odpor
Mobilné zariadenie
Napájací zdroj
Napäťový chránič
Napäťový násobič
Nortonova veta
Odpínač
Odpojovač
OLED
Olovený akumulátor
Paralelné zapojenie
Peltierov článok
Plošná hustota elektrického prúdu
Poistka (elektrotechnika)
Posuvný prúd
Prúdový chránič
Prenosové médium
Prieletový klystrón
Primárny elektrochemický článok
Reaktancia
Rekuperácia (dopravný prostriedok)
Relé
Reproduktorová výhybka
Rezistancia
Rozhranie (interface)
Sériové zapojenie
Seebeckov jav
Sekundárny elektrochemický článok
Settopbox
Skrat
Sonar
Spínač
Spínaný zdroj
Straty v mikropásikových vedeniach
Striedavý prúd
Stupeň ochrany krytom
Svetelná výbojka
Symetrizačný člen
Technická normalizácia
Tepelné relé
Tepelne vodivostný detektor
Termočlánok
Théveninova veta
Transformátor
Transformátor s fázovou reguláciou
Trojfázová sústava
Tuhá fáza (elektronika)
Tyratrón
Usmerňovač (elektrotechnika)
Uzemnenie
Uzol (vodiče)
Vírivý prúd
Výbojka
Varistor
Ventilátor
Vodič (elektrotechnika)
Voltov stĺp
Vstavaný systém
Zásuvka (elektrotechnika)
Zdroj (elektrotechnika)
Zisk antény
Text je dostupný za podmienok Creative
Commons Attribution/Share-Alike License 3.0 Unported; prípadne za ďalších
podmienok.
Podrobnejšie informácie nájdete na stránke Podmienky
použitia.
www.astronomia.sk | www.biologia.sk | www.botanika.sk | www.dejiny.sk | www.economy.sk | www.elektrotechnika.sk | www.estetika.sk | www.farmakologia.sk | www.filozofia.sk | Fyzika | www.futurologia.sk | www.genetika.sk | www.chemia.sk | www.lingvistika.sk | www.politologia.sk | www.psychologia.sk | www.sexuologia.sk | www.sociologia.sk | www.veda.sk I www.zoologia.sk